题目内容
【题目】微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也应用广泛。
(1)基态B原子的电子排布图为________________________,其第一电离能比Be___________(填“大”或“小”)。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构简式为___________ (标出配位键),其中心原子的杂化方式为________,写出[BH4]-的一种阳离子等电子体_______。
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为____________(以n表示硼原子的个数)。

(4)硼酸晶体是片层结构,下图表示的是其中一层的结构。每一层内存在的作用力有_________。

(5)三氯化硼的熔点比氯化镁的熔点低,原因是_______________________。
(6)镁单质晶体中原子的堆积模型如下图,它的堆积模型名称为_______;紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏伽德罗常数为NA,则镁的摩尔质量的计算式是________________。

【答案】![]() 小
小 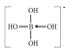 sp3 NH4+ (BO2)nn- 共价键、氢键 三氯化硼为分子晶体,而氯化镁为离子晶体,范德华力比离子键弱 六方最密堆积 12NA·a·ρ
sp3 NH4+ (BO2)nn- 共价键、氢键 三氯化硼为分子晶体,而氯化镁为离子晶体,范德华力比离子键弱 六方最密堆积 12NA·a·ρ
【解析】
(1)基态B原子的核电荷数为5,基态B的电子排布式为1s22s22p1;Be原子元素2s轨道为全充满稳定状态,第一电离能高于同周期相邻元素的;
(2)硼化合物是典型的缺电子结构化合物,H3BO3也属于缺电子化合物,可接受OH-的一对孤电子对形成B(OH)4-;中心原子B键合电子对数目为4,没有孤电子对;等电子体是指原子数目相同,价电子总数相同的微粒;
(3)根据均摊思想分析偏硼酸根离子的化学式;
(4)硼酸晶体是片层结构,硼酸分子内存在共价键,分子间存在氢键,分子之间还存在范德华力;
(5)三氯化硼是共价型分子,而氯化镁是离子化合物;
(6)镁单质晶体中原子的堆积方式是按ABABABAB…的方式堆积;根据晶胞的结构可知紧邻的四个镁原子的中心连线构成的几何体占整个晶胞的![]() ,而晶胞中含有的镁原子数为1+
,而晶胞中含有的镁原子数为1+![]() ×8=2,根据ρ=
×8=2,根据ρ= ,即可计算Mr。
,即可计算Mr。
(1)基态B的电子排布式为1s22s22p1,由泡利原理、洪特规则,电子排布图为![]() ;Be原子元素2s轨道为全充满稳定状态,第一电离能高于同周期相邻元素的,故第一电离能Be>B;
;Be原子元素2s轨道为全充满稳定状态,第一电离能高于同周期相邻元素的,故第一电离能Be>B;
(2)硼化合物是典型的缺电子结构化合物,H3BO3也属于缺电子化合物,可接受OH-的一对孤电子对形成B(OH)4-,所以形成配位键,表示为: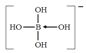 ;B键合电子对数目为4,没有孤电子对,则中心原子的杂化方式为sp3;等电子体是指原子数目相同,价电子总数相同的微粒,则与[BH4]-互为等电子体的阳离子有:NH4+;
;B键合电子对数目为4,没有孤电子对,则中心原子的杂化方式为sp3;等电子体是指原子数目相同,价电子总数相同的微粒,则与[BH4]-互为等电子体的阳离子有:NH4+;
(3)根据均摊思想,无限长链式偏硼酸根离子中,一个B相当于占有O的数目为1+2×![]() =2,所以其化学式可表示为:(BO2)nn-;
=2,所以其化学式可表示为:(BO2)nn-;
(4)硼酸晶体是片层结构,硼酸分子内存在共价键,分子间存在氢键,分子之间还存在范德华力;
(5)三氯化硼是共价型分子,其晶体为分子晶体,而氯化镁是离子化合物,其晶体是离子晶体,因范德华力比离子键弱,则三氯化硼的熔点比氯化镁的熔点低;
(6)镁单质晶体中原子的堆积方式是按ABABABAB…的方式堆积,是六方最密堆积;根据晶胞的结构可知紧邻的四个镁原子的中心连线构成的几何体占整个晶胞的![]() ,而晶胞中含有的镁原子数为1+
,而晶胞中含有的镁原子数为1+![]() ×8=2,根据ρ=
×8=2,根据ρ= ,则有Mr=12NAaρ。
,则有Mr=12NAaρ。

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案【题目】三氯乙醛(CCl3CHO)是生产农药、医药的重要中间体,实验室制备三氯乙醛的反应装置示意图(加热装置未画出)和有关数据如下:
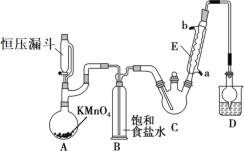
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②相关物质的相对分子质量及部分物理性质:
相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
C2H5OH | 46 | -114.1 | 78.3 | 与水互溶 |
CCl3CHO | 147.5 | -57.5 | 97.8 | 可溶于水、乙醇 |
CCl3COOH | 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 |
C2H5Cl | 64.5 | -138.7 | 12.3 | 微溶于水,可溶于乙醇 |
(1)恒压漏斗中盛放的试剂的名称是_____,盛放KMnO4仪器的名称是_____。
(2)反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸),写出三氯乙醛被次氯酸氧化生成三氯乙酸的化学方程式:_____。
(3)该设计流程中存在一处缺陷是_____,导致引起的后果是_____,装置B的作用是______。
(4)反应结束后,有人提出先将C中的混合物冷却到室温,再用分液的方法分离出三氯乙酸。你认为此方案是否可行_____(填是或否),原因是_____。
(5)测定产品纯度:称取产品0.36g配成待测溶液,加入0.1000molL1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000molL1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为_____(计算结果保留四位有效数字)。滴定原理:CCl3CHO+OH-=CHCl3+HCOO-、HCOO-+I2=H++2I-+CO2、I2+2S2O32-=2I-+S4O62-