题目内容
4.用18mol•L-1 浓硫酸配制100mL 3.0mol•L-1 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解④转移、洗涤 ⑤定容、摇匀
完成下列问题:
(1)配制该溶液除烧杯、量筒、玻璃棒外,还需用到的仪器有100mL容量瓶和胶头滴管
(2)所需浓硫酸的体积是16.7mL,量取浓硫酸所用的量筒的规格是B
(从下列中选用 A.10mL B.25mL C.50mL D.100mL).
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
①容量瓶用蒸馏洗涤后残留有少量的水无影响
②用量筒量取浓硫酸是俯视读数偏小.
分析 (1)根据配制一定物质的量浓度的溶液的步骤是称量、量取、稀释、移液、洗涤、定容、摇匀和装瓶来分析所需的仪器;
(2)根据稀释定律来计算所需的浓硫酸的体积;根据大而近的原则来分析所选用的量筒的规格;
(3)分析具体操作对n、V的影响,根据c=分析不当操作对溶液浓度的影响.
解答 解:(1)根据配制一定物质的量浓度的溶液的步骤是称量、量取、稀释、移液、洗涤、定容、摇匀和装瓶可知所需的仪器有:量筒、烧杯、玻璃棒、100mL容量瓶和胶头滴管,故除烧杯、量筒、玻璃棒外,还需用到的仪器有100mL容量瓶和胶头滴管,故答案为:100mL容量瓶和胶头滴管;
(2)设需要的浓硫酸的体积为VmL,根据稀释定律可知:18mol/L×VmL=3mol/L×100mL,解得V=16.7mL;根据大而近的原则,应选择25mL量筒,
故答案为:16.7mL;B;
(3)①容量瓶用蒸馏洗涤后残留有少量的水,对溶液浓度无影响,故答案为:无影响;
②用量筒量取浓硫酸是俯视读数,则浓硫酸的体积偏小,浓度偏低,故答案为:偏小.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,难度不大,掌握公式的运用和配制原理是解题的关键.

练习册系列答案
相关题目
12.下列反应无论怎样调整反应物的用量,都只能生成一种物质的是( )
| A. | 甲烷与氯气混合后在光照的条件下发生反应 | |
| B. | 乙烯与水的加成反应 | |
| C. | 甲苯与浓硝酸发生硝化反应 | |
| D. | 2,3-二溴丁烷的消去反应 |
19.NA 表示阿伏加德罗常数,则下列说法正确的是( )
| A. | 22.4L CO中一定含有6.02×1023个分子 | |
| B. | 在标准状况下,22.4L CH4与18g H2O所含有的电子数均为10 NA | |
| C. | 常温常压下,16g O2 与16gO3含有的分子数相同 | |
| D. | 0.1 mol/L K2SO4 溶液中含有 K+为0.2 NA |
9.下列各组物质,用一种试剂无法区别的是( )
| A. | 三种浓酸:HNO3、H2SO4、HCl | |
| B. | 四种黑色粉末:FeO、Fe、CuO、C | |
| C. | 四种无色溶液:NaCl、NaOH、KOH、KCl | |
| D. | 四种白色粉末:(NH4)2SO4、NH4Cl、Na2SO4、NaCl |
16.某烃的结构简式为: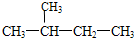 ,它的名称是( )
,它的名称是( )
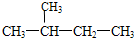 ,它的名称是( )
,它的名称是( )| A. | 3-甲基戊烷 | B. | 2,3-二甲基丙烷 | C. | 2-甲基丁烷 | D. | 3-甲基丁烷 |
13.假设体积可以相加,下列叙述中正确的是( )
| A. | pH=12的氨水,加水稀释100倍后溶液pH=10 | |
| B. | 90℃纯水的pH=6.2,则说明加热可导致水呈酸性 | |
| C. | 0.1mol•L-1的硫酸,与等体积水混合后溶液pH=1(假设混合后溶液的体积不变) | |
| D. | pH=3的盐酸与pH=11的氨水等体积混合后pH=7 |