题目内容
【题目】如图所示,从A处通入Cl2。当关闭B阀时,C处的红布逐渐褪色;当打开B阀后,C处的红布无明显现象,则下列判断正确的是
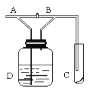
A.通入的Cl2可能是潮湿的B.红布一定是干燥的
C.D中的液体可能是NaOHD.使红布褪色的物质是Cl2
【答案】B
【解析】
氯气与水反应可以产生次氯酸,次氯酸具有漂白作用,能够使红色布条褪色;干燥的氯气不能使干燥的红色布条褪色,所以干燥的氯气无漂白作用;当打开B阀后,C处的红布无明显现象,红布一定是干燥的,故B正确、A、D错误;当关闭B阀时,C处的红布逐渐褪色,说明氯气可以通过D中的溶液进入C内,由于氯气在水中的溶解度较小,且与水的反应程度很小,所以D中可以盛装的是水;而氯气与氢氧化钠反应,氯气被吸收,没有氯气逸出,所以D装置不能盛装氢氧化钠溶液,故C错误;结合以上分析可知,B选项正确;
故答案选B。

【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 元素原子的核外p电子数比s电子数少1个 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
(1)写出下列元素符号:A______, B_______,C________,D__________。
(2)写出C元素在周期表的位置_________,E2+价电子的轨道表示式______________,B元素能量最高的电子为____轨道上的电子,其轨道呈______形。
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______个,π键有______个。(阿伏加德罗常数的值用NA表示)
(4)B、C、D的简单离子的半径由大到小的顺序为________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________。