题目内容
【题目】用1L1mol/L的NaOH溶液吸收0.8molCO2,求所得的溶液中CO32-和HCO3-的物质的量之比为___________
【答案】1:3
【解析】
1L 1mol/L NaOH溶液含1molNaOH,
设生成xmolNa2CO3,ymoNaHCO3,根据Na、C守恒,
列式:x+y=0.8mol,2x+y=1mol,计算即可。
1L 1mol/L NaOH溶液含1molNaOH,
设生成xmolNa2CO3,ymoNaHCO3,根据Na、C守恒,
列式:x+y=0.8mol,2x+y=1mol
解得x=0.2mol,y=0.6mol,溶液中CO32与HCO3的物质的量浓度之比1:3;
故答案为:1:3。

 名校课堂系列答案
名校课堂系列答案【题目】已知标准状况下22.4LCO和CO2混合气体的质量为40g.将此混合气体通入1L1mol/LNaOH溶液充分反应,生成的盐用A、B表示.请将生成盐的化学式及质量填入右表(若只生成一种盐,此表不用填满).
生成的盐 | 化学式 | 质量/g |
A | ||
B |
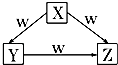
【题目】X、Y、Z、W是中学化学常见的四种物质,它们之间具有如图所示转化关系,则下列组合不可能的是( )
X | Y | Z | W | |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAlO2 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
A.A
B.B
C.C
D.D
【题目】四种常见元素的性质或结构信息如表,根据信息回答有关问题.
元素 | A | B | C | D |
性质 | 原子核外有两个电子层,最外层有3个未成对电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为:[Ar]3 d104sx , 有+1、+2两种常见化合价 | 有两种常见氧化物,其中一种是冶炼金属工业的常用还原剂 |
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为(用元素符号表示);试解释原因 .
(2)B元素的低价氧化物分子中心原子的杂化方式为 , B元素的最高价氧化物分子的VSEPR构型为;B元素与D元素形成分子空间构型为;
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点(填“高”或“低”),其原因是;
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为;后一现象的离子方程式为: .
(5)C晶体的堆积方式如图所示 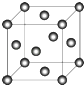 ,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为 , C晶体的密度为gcm﹣3(要求写表达式,可以不简化).
,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为 , C晶体的密度为gcm﹣3(要求写表达式,可以不简化).