题目内容
9.下列说法正确的是( )| A. | 根据分散系的稳定性,将分散系分为溶液、胶体和浊液 | |
| B. | 根据是否具有丁达尔效应鉴别蛋白质溶液和氯化钠溶液 | |
| C. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,生成Fe(OH)3胶体 | |
| D. | “纳米材料”是粒子直径为1 nm~100 nm的材料,纳米铜是其中的一种,它是胶体 |
分析 A.根据分散系微粒直径的大小,将分散系分为溶液、胶体和浊液;
B.胶体分散系具有丁达尔现象,溶液没有;
C.氯化铁溶液中逐滴加入NaOH溶液,会发生复分解反应产生红褐色沉淀;
D.胶体是分散系.
解答 解:A.根据分散系微粒直径的大小,将分散系分为溶液、胶体和浊液,不是根据稳定性,故A错误;
B.蛋白质溶液是胶体,氯化钠溶液是溶液,可通过丁达尔效应来鉴别蛋白质溶液和氯化钠溶液,故B正确;
C.氯化铁溶液中逐滴加入NaOH溶液,会发生复分解反应产生红褐色沉淀,不涉及胶体性质,故C错误;
D.胶体是分散系,纳米材料不是胶体,故D错误.
故选B.
点评 本题考查胶体的性质,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.请回答:
Ⅰ:C、N、O、Al、Si、Cu是常见的六种元素.
(1)Si位于元素周期表第三周期第IVA族.
(2)N的基态原子核外电子排布式为1s22s22p3;Cu的基态原子最外层有1个电子.
(3)用“>”或“<”填空:
Ⅱ:
(4)H2O2的电子式 .
.
(5)镁燃烧不能用CO2灭火,用化学方程式表示其理由2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(6)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式AgCl(s)+Br-═AgBr(s)+Cl-.
(7)完成以下氧化还原反应的离子方程式:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
Ⅰ:C、N、O、Al、Si、Cu是常见的六种元素.
(1)Si位于元素周期表第三周期第IVA族.
(2)N的基态原子核外电子排布式为1s22s22p3;Cu的基态原子最外层有1个电子.
(3)用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al>Si | N<O | 金刚石>晶体硅 | CH4<SiH4 |
(4)H2O2的电子式
 .
.(5)镁燃烧不能用CO2灭火,用化学方程式表示其理由2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(6)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式AgCl(s)+Br-═AgBr(s)+Cl-.
(7)完成以下氧化还原反应的离子方程式:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
17.下列有关物质的性质或应用的说法不正确的是( )
| A. | 石油裂化可获得乙烯、丙烯和丁二烯 | |
| B. | 水玻璃可用于生产黏合剂和防火剂 | |
| C. | 盐析可提纯蛋白质并保持其生理活性 | |
| D. | 二氧化硅是生产光纤制品的基本原料 |
14.下列物质在氢氧化钠溶液和加热条件下反应后生成的对应有机物中,能够能被催化氧化成醛的是( )
| A. | (CH3)2CHCl | B. | CH3C(CH3)2I | C. | (CH3)3CCOOCH2CH3 | D. | CH3C(CH3)2CH2Br |
18.下列各组元素性质的递变情况错误的是( )
| A. | Na、Mg、Al原子最外层电子数依次增多 | |
| B. | N、O、F元素最高正价依次增大 | |
| C. | Na、K、Rb电负性逐渐减小 | |
| D. | P、S、Cl元素最高价含氧酸酸性依次增强 |
19.下列性质的比较中,正确的是( )
| A. | 碱性:KOH>NaOH>Mg(OH)2>Ca(OH)2 | B. | 沸点:HF<HCl<HBr<HI | ||
| C. | 热稳定性:CH4>PH3>H2O>HF | D. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
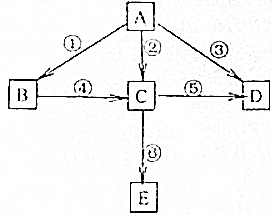 己知A为单质,B、C、D、E为化合物.它们之间存在如图转化关系:
己知A为单质,B、C、D、E为化合物.它们之间存在如图转化关系: 高锰酸钾是一种重要的化学试剂,其溶液不很稳定,在酸性条件下会分解生成二氧化锰和氧气,在中性或弱碱性溶液中分解速度很慢,见光分解速度加快.
高锰酸钾是一种重要的化学试剂,其溶液不很稳定,在酸性条件下会分解生成二氧化锰和氧气,在中性或弱碱性溶液中分解速度很慢,见光分解速度加快. ;
;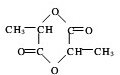 +2H2O;
+2H2O;