题目内容
在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的体积和所得沉淀的物质的量的关系如下图所示(b处NaOH溶液的体积为1L),则下列判断不正确的是 ( )
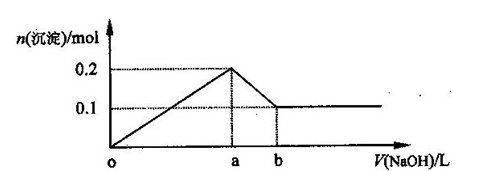

| A.NaOH的浓度为0.6 mol/L | B.在a点处溶液中的溶质为NaCl |
| C.在b点处溶液中的溶质只有NaAlO2 | D.图中线段oa : ab=5 : 1 |
C
从图像可知,Mg(OH)2的物质的量为0.1mol,Al(OH)3的物质的量为0.1mol,在b点共消耗NaOH 0.6mol,b处NaOH溶液的体积为1L,所以,NaOH的浓度为0.6 mol/L,A 正确。
在a点,Mg2+、Al3+都是以离子形式存在,溶液中阳离子只有Na+,故在a点处溶液中的溶质为NaCl,B 正确。
在b点处溶液中的溶质有NaAlO2和NaCl,C 错误。
oa段消耗OH-0.5mol,ab段消耗OH-0.1mol,故oa : ab=5 : 1 D正确。
在a点,Mg2+、Al3+都是以离子形式存在,溶液中阳离子只有Na+,故在a点处溶液中的溶质为NaCl,B 正确。
在b点处溶液中的溶质有NaAlO2和NaCl,C 错误。
oa段消耗OH-0.5mol,ab段消耗OH-0.1mol,故oa : ab=5 : 1 D正确。

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
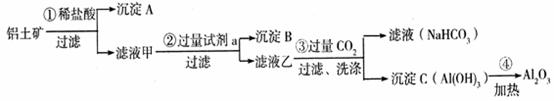
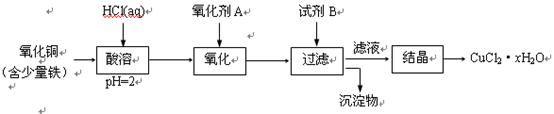

 积关系;如图所示。计算:
积关系;如图所示。计算:

 3 ②(NH4)2S ③Al2O3 ④Al(OH)3 ⑤Al
3 ②(NH4)2S ③Al2O3 ④Al(OH)3 ⑤Al