题目内容
在标准状况下,将CO2和CO的混合气(密度为 g·L-1)充满一盛有足量Na2O2的密闭容器中(见下图所示),容器容积为22.4L(不计固态物质的体积)。用间断而短暂的电火花引发反应,令容器内可能发生的反应都充分进行(反应均系两物质之间的)。通过计算判断下列说法中正确的有( )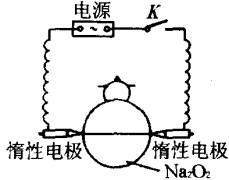
①反应前CO2和CO的物质的量分别0.25mol和0.75mol
②反应完成后容器内有0.5mol CO
③反应完成后容器内有0.125mol O2
④反应完成后容器内有0.25mol Na2CO3
⑤反应完成后容器内有0.5mol Na2CO3
A.①② B.①③
C.①④ D.③⑤
答案:B
提示:
提示:
| 解法一: 气体总物质的量=1mol
容器中所发生的反应为:2Na2O2+2CO2==2Na2CO3+O2, 2CO+O2==2CO2 两反应循环进行,联立得: Na2O2+CO==Na2CO3 即可理解为:Na2O2足量前提下,在CO2作用下,Na2O2可将CO全部吸收生成Na2CO3,CO2也被Na2O2吸收生成Na2CO3和O2。 ∴反应完成后,容器中有O2和Na2CO3。 依据碳守恒: n(Na2CO3)=n(CO)+n(CO2)=1mol n( 解法二:由混合气体平均相对分子质量为32,用十字交叉法求CO、CO2的物质的量的比: 其他同上。 用物质的量和质量列方程求解。 对循环进行的反应,反应方程式可相加处理。如:2Na2O2+2CO2==2Na2CO3+O2,2CO+O2=2CO2, 相加得:Na2O2+CO==Na2CO3
|

练习册系列答案
 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
