题目内容
【题目】下列指定化学用语正确的是
A.NaHS水解的离子方程式:HS-+H2O=S2-+H3O+
B.Ba(OH)2的电离方程式:Ba(OH)2![]() Ba2++2OH-
Ba2++2OH-
C.NaHSO4在水中的电离方程式:NaHSO4=Na++H++SO42-
D.Na2S水解的离子方程式:S2-+2H2O=H2S+2OH-
【答案】C
【解析】
A.水解为可逆反应,正确的离子方程式应为HS-+H2O![]() S2-+H3O+,故A错误;
S2-+H3O+,故A错误;
B.Ba(OH)2为强电解质,在水溶液中完全电离,电离方程式为Ba(OH)2=Ba2++2OH-,故B ;
C.NaHSO4为强电解质,且硫酸为强酸,硫酸氢根在水溶液中完全电离,所以硫酸氢钠在水溶液中电离方程式为:NaHSO4=Na++H++SO42-,故C正确;
D.H2S为二元弱酸,所以S2-分步水解,且以第一步水解为主,所以Na2S水解的离子方程式为S2-+H2O=HS-+OH-,故D错误;
故答案为C。

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
【题目】用如图中装置进行实验,实验一段时间后,现象与预测不一致的是
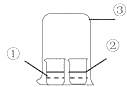
①中物质 | ②中物质 | 实验预测 | |
A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
A. AB. BC. CD. D