题目内容
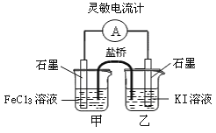
【题目】按如图所示,两个烧杯中分别盛有足量的稀硫酸和氯化铜溶液:

(1)A、B两个装置中,属于原电池的是_________(填标号)。
(2)A池中,铜极为_________极,发生_________反应(填“氧化”或“还原”),电极反应式为__________________。
(3)B池中,左边C是_________极,电极反应式为__________________________________________________,总反应式为___________________________________________________________。
(4)B池中当阴极产生6.4g铜时,阳极放出_________g气体。
【答案】(1)A (2)正;还原;2H++2e-=H2↑(3)阳极;2Cl--2e-=Cl2↑;CuCl2![]() Cu+Cl2↑
Cu+Cl2↑
(4)7.1
【解析】
(1)装置A中没有外接电源,是原电池,B是电解池。
(2)在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,铜是正极,溶液中的氢离子在正极得到电子,发生还原反应产生氢气。
(3)左侧电极和电源的负极相连,作阳极,溶液中的氯离子放电,产生氯气。阳极阴极是铜离子放电,析出铜,所以总反应式为CuCl2![]() Cu+Cl2↑。
Cu+Cl2↑。
(4)生成6.4g铜转移的电子是6.4g÷64g/mol×2=0.2mol。根据电子的得失守恒可知,阳极产生的氯气是0.2mol÷2=0.1mol,质量是0.1mol×71g/mol=7.1g。

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目