题目内容
下列离子方程式正确的是( )
| A、澄清石灰水加入稀盐酸 Ca(OH)2+2H+=Ca2++2H2O |
| B、钠与水反应 Na+2H2O=Na++2OH-+H2↑ |
| C、铜插入硝酸银溶液 Cu+Ag+=Cu2++Ag |
| D、大理石溶于醋酸CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.澄清石灰水中,氢氧化钙在离子方程式中需要拆开,写成离子形式;
B.根据电荷守恒判断,该离子方程式两边电荷不守恒;
C.根据电荷守恒判断,离子方程式两边正负电荷不相等;
D.醋酸为弱酸、碳酸钙为难溶物,二者在离子方程式中都需要保留化学式.
B.根据电荷守恒判断,该离子方程式两边电荷不守恒;
C.根据电荷守恒判断,离子方程式两边正负电荷不相等;
D.醋酸为弱酸、碳酸钙为难溶物,二者在离子方程式中都需要保留化学式.
解答:
解:A.澄清石灰水加入稀盐酸,反应生成氯化钙和水,氢氧化钙应该拆开,正确的离子方程式为:OH-+H+=H2O,故A错误;
B.钠与水反应生成氢氧化钠和氢气,离子方程式必须满足电荷守恒,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.铜与硝酸银反应生成硝酸铜和银单质,离子方程式电荷不守恒,正确的离子方程式为:Cu+2Ag+=Cu2++2Ag,故C错误;
D.大理石的主要成分为碳酸钙,碳酸钙与醋酸都需要保留化学式,反应的离子方程式为:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O,故D正确;
故选D.
B.钠与水反应生成氢氧化钠和氢气,离子方程式必须满足电荷守恒,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.铜与硝酸银反应生成硝酸铜和银单质,离子方程式电荷不守恒,正确的离子方程式为:Cu+2Ag+=Cu2++2Ag,故C错误;
D.大理石的主要成分为碳酸钙,碳酸钙与醋酸都需要保留化学式,反应的离子方程式为:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O,故D正确;
故选D.
点评:本题考查了离子方程式的正误判断,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列关于煤和石油的说法正确的是( )
| A、煤和石油均属于可再生矿物能源 |
| B、煤经干馏再分馏可获得芳香烃 |
| C、石油分馏得到的各馏分均是纯净物 |
| D、石油裂解的目的是为了提高汽油的产量与质量 |
下列各组物质中,不管它们以何种比例混合,只要总物质的量一定,充分燃烧后消耗氧气的量一定的是( )
| A、C2H2和C6H6 |
| B、C2H6O和C3H6O2 |
| C、CH2O和C2H4O2 |
| D、C3H8和C4H8O2 |
m g铜和足量的浓硫酸反应,生成SO2 n L,则被还原的硫酸是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
分离淀粉与食盐的混合溶液,可采取的方法是( )
| A、蒸发、结晶 |
| B、渗析 |
| C、加AgNO3溶液、过虑 |
| D、萃取 |
下列微粒的核外电子的表示方法中正确的是( )
A、基态碳原子的电子排布图 |
B、基态铜原子核外的3d、4s轨道内电子排布图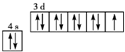 |
| C、Cl的外围电子排布式3s13p6 |
| D、Fe2+的电子排布式1s22s22p63s23p63d6 |
下列各组物质既能与强酸反应,且受热后能产生刺激性气味气体的是( )
| A、氯化铵溶液 |
| B、碳酸氢钾溶液 |
| C、碳酸氢铵溶液 |
| D、硫酸氢钠溶液 |
NA代表阿伏加德罗常数的值.下列叙述中正确的是( )
| A、标准状况下,2.24L CH2Cl2含有分子的数目为0.1NA |
| B、常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
| C、在标准状况下,11.2L NO与11.2L O2混合后气体分子数为0.75NA |
| D、1mol FeCl3完全水解得到的Fe(OH)3胶体中含有的胶粒的数目为1NA |
下列能源中,属于无污染能源的是( )
| A、煤气 | B、核能 | C、太阳能 | D、石油 |