题目内容
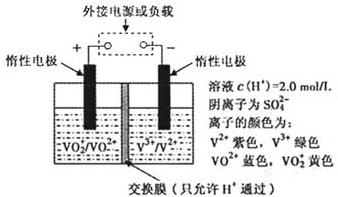
 全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能的相互转化,其原理如图所示.(已知V2+呈紫色,V3+呈绿色;VO2+呈蓝色,VO2+呈黄色.溶液中c(H+)=2.0mol/L,阴离子为SO42-.)
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能的相互转化,其原理如图所示.(已知V2+呈紫色,V3+呈绿色;VO2+呈蓝色,VO2+呈黄色.溶液中c(H+)=2.0mol/L,阴离子为SO42-.)(1)电池放电时,左槽溶液由黄色变为蓝色.
①左槽的电极反应式为
②外加负载为浸有KI淀粉试液的滤纸,则滤纸的
(2)电池充电时,外加电源的
(3)放电过程中,H+的作用为
(4)充电时,若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为
分析:(1)①左槽溶液逐渐由黄变蓝,VO2+转变为VO2+,发生还原反应,应为原电池的负极;
②外加负载为浸有KI淀粉试液的滤纸,是电解装置,碘离子移向阳极A电极失电子生成碘单质,遇淀粉变蓝;
(2)充电过程中,右槽连接电源的负极,发生还原反应,为电解池的阴极,电极反应式为V3++e-═V2+;
(3)放电过程中氢离子在正极参与电极反应,同时通过交换膜定向移动使电流通过溶液;
(4)充电时,左槽发生的反应为VO2++H2O-e-═VO2++2H+,当转移电子为3.01×1023个即为0.5 mol电子时,生成氢离子为1mol.
②外加负载为浸有KI淀粉试液的滤纸,是电解装置,碘离子移向阳极A电极失电子生成碘单质,遇淀粉变蓝;
(2)充电过程中,右槽连接电源的负极,发生还原反应,为电解池的阴极,电极反应式为V3++e-═V2+;
(3)放电过程中氢离子在正极参与电极反应,同时通过交换膜定向移动使电流通过溶液;
(4)充电时,左槽发生的反应为VO2++H2O-e-═VO2++2H+,当转移电子为3.01×1023个即为0.5 mol电子时,生成氢离子为1mol.
解答:解:(1)①当左槽溶液逐渐由黄变蓝,其电极反应式为VO2++2H++e-═VO2++H2O,电池放电时,说明此时为原电池,且为原电池的正极.
故答案为:VO2++2H++e-═VO2++H2O;
②外加负载为浸有KI淀粉试液的滤纸,是电解装置,碘离子移向阳极A电极失电子生成碘单质,2I-=2e-═I2,遇淀粉变蓝,所以滤纸A端先变蓝,
故答案为:A;
(2)充电过程中,A为正极,右槽连接的是电源负极,为电解池的阴极,电极反应式为V3++e-═V2+,V3+为绿色,V2+为紫色,故可以看到右槽溶液颜色逐渐由绿色变为紫色,
故答案为:A;绿色逐渐变为紫色;
(3)放电过程中,电极反应式为VO2++2H++e-═VO2++H2O,氢离子的作用是充电是,参与正极反应,通过交换膜定向移动使电流通过溶液,
故答案为:氢离子在正极参与电极反应,同时通过交换膜定向移动使电流通过溶液;
(4)充电时,左槽发生的反应为VO2++H2O═VO2++2H++e-,当转移电子为3.01×1023个即为0.5 mol电子时,生成氢离子为1 mol,此时氢离子参与正极反应,通过交换膜定向移动使电流通过溶液,溶液中离子的定向移动可形成电流,通过0.5mol电子,有0.5mol氢离子移向阴极,则左槽溶液中n(H+)的变化量为1mol-0.5mol=0.5mol,
故答案为:0.5mol.
故答案为:VO2++2H++e-═VO2++H2O;
②外加负载为浸有KI淀粉试液的滤纸,是电解装置,碘离子移向阳极A电极失电子生成碘单质,2I-=2e-═I2,遇淀粉变蓝,所以滤纸A端先变蓝,
故答案为:A;
(2)充电过程中,A为正极,右槽连接的是电源负极,为电解池的阴极,电极反应式为V3++e-═V2+,V3+为绿色,V2+为紫色,故可以看到右槽溶液颜色逐渐由绿色变为紫色,
故答案为:A;绿色逐渐变为紫色;
(3)放电过程中,电极反应式为VO2++2H++e-═VO2++H2O,氢离子的作用是充电是,参与正极反应,通过交换膜定向移动使电流通过溶液,
故答案为:氢离子在正极参与电极反应,同时通过交换膜定向移动使电流通过溶液;
(4)充电时,左槽发生的反应为VO2++H2O═VO2++2H++e-,当转移电子为3.01×1023个即为0.5 mol电子时,生成氢离子为1 mol,此时氢离子参与正极反应,通过交换膜定向移动使电流通过溶液,溶液中离子的定向移动可形成电流,通过0.5mol电子,有0.5mol氢离子移向阴极,则左槽溶液中n(H+)的变化量为1mol-0.5mol=0.5mol,
故答案为:0.5mol.
点评:本题考查了原电池中负极失去电子,为还原剂发生氧化反应,正极得到电子,为氧化剂发生还原反应,在电解池中,与电源正极相连为阳极,发生氧化反应,失去电子,与电源负极相连的阴极,发生还原反应,得到电子,题目难度中等.

练习册系列答案
相关题目
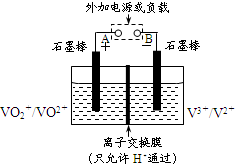
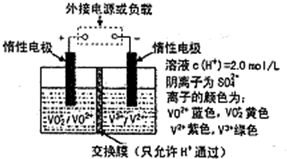
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示:
下列说法错误的是( )

下列说法错误的是( )
A、当左槽溶液逐渐由黄变蓝,其电极反应式为VO
| ||
| B、充电时若转移的电子数为3.01×1023,则左槽溶液中行n(H+)最终的变化量为1mol | ||
| C、放电过程中,氢离子的作用之一是参与正极反应 | ||
| D、充电过程中,右槽溶液颜色逐渐由绿色变为紫色 |
 钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.V2O5是接触法制硫酸的催化剂.
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.V2O5是接触法制硫酸的催化剂.