题目内容
【题目】有几种元素的微粒的电子层结构为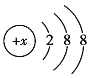 ,试回答下列问题:
,试回答下列问题:
(1)若该微粒代表一种原子,则这种微粒的符号是______;
(2)向该微粒(带负电荷)的盐溶液中加入![]() 溶液时会出现白色沉淀,则这种微粒的符号是______;
溶液时会出现白色沉淀,则这种微粒的符号是______;
(3)某原子失去一个电子形成该微粒,则这种微粒的符号是______;
(4)某原子得到两个电子形成该微粒,则这种微粒的符号是______。
【答案】![]()
![]()
![]()
![]()
【解析】
由该微粒的结构示意图可知,可能是18号元素氩原子或周期表中相邻元素,包括金属的阳离子或非金属的阴离子。
(1)由该原子性质可知及核外电子总数知道,该原子质子数为18,故该原子为氩原子:Ar;
(2)盐溶液中的某微粒与AgNO3溶液反应时会出现白色沉淀,则该微粒是Cl,氯离子和银离子反应:Ag++Cl=AgCl↓,生成AgCl白色沉淀;
(3)该元素原子核外有19个电子,即钾原子,这种微粒的钾离子:K+;
(4)该元素原子核外有16个电子,即硫原子,这种微粒的硫离子:S2。

【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价(已知铍的原子半径为0.089 nm)。
元素代号 | A | B | C | D | E |
原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
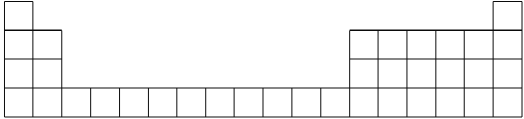
(1)用元素代号标出它们在周期表中所对应的位置(以下为周期表的一部分)_________。
(2)画出A的原子结构示意图_________。
(3)B元素处于周期表中第________周期,________族。
(4)E元素处于周期表中第________周期,________族。
(5)C、D的简单离子的半径由大到小顺序为________(用离子符号表示)。
(6)上述五种元素的最高价氧化物对应的水化物中酸性最强的是__________(填化学式)。
(7)C、E形成的化合物为________(填化学式)。
(8)写出B单质和氢氧化钠溶液反应的方程式__________写出B的最高价氧化物对应水化物和氢氧化钠溶液反应的离子方程式:________
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 是四种短周期元素,它们的核电荷数依次增大,四种元素的性质或原子结构的部分信息如表所示。
是四种短周期元素,它们的核电荷数依次增大,四种元素的性质或原子结构的部分信息如表所示。
元素 | 元素性质或原子结构的部分信息 |
| 元素的离子核外无电子 |
| 地壳中含量最多的元素 |
| 元素的离子半径在该周期中最小 |
|
|
下列叙述不正确的是( )
A.![]() 与
与![]() 形成的化合物在常温下为气体
形成的化合物在常温下为气体
B.![]() 的最高价氧化物对应的水化物不与
的最高价氧化物对应的水化物不与![]() 溶液反应
溶液反应
C.![]() 和
和![]() 形成的常见化合物能形成酸雨
形成的常见化合物能形成酸雨
D.简单氢化物的稳定性:![]()
