题目内容
【题目】根据要求填空
(1)Mg2+的结构示意图________,O原子的电子式__________,NH3的结构式 _________。
(2)MgO 的电子式____________,Mg(NO3)2的式量是 _____________。
(3)约含有3.01×1022个NO分子的质量为_____g,在标准状态下所占的体积约为_____L。
【答案】
![]()
![]() Mg2+
Mg2+  148 1.5 1.12
148 1.5 1.12
【解析】
(1)Mg2+的质子数为12,电子数为10,用小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数;氧原子最外层为6个电子,据此书写电子式;
(2)MgO是由镁离子和氧离子构成的离子化合物;Mg(NO3)2的摩尔质量为148g/mol;
(3)约含有3.01×1022个NO分子的物质的量为3.01×1022/6.02×1023=0.05mol。
(1)Mg2+的质子数为12,电子数为10,离子结构示意图为![]() ;氧原子最外层为6个电子,O的电子式为:
;氧原子最外层为6个电子,O的电子式为:![]() ;NH3为四核十电子分子,分子中有3对共用电子对,则结构式为
;NH3为四核十电子分子,分子中有3对共用电子对,则结构式为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;![]() ;
;
(2)MgO是由镁离子和氧离子构成的离子化合物,电子式为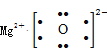 ;Mg(NO3)2的摩尔质量为148g/mol,式量为148,故答案为:
;Mg(NO3)2的摩尔质量为148g/mol,式量为148,故答案为: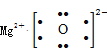 ;148;
;148;
(3)约含有3.01×1022个NO分子的物质的量为3.01×1022/6.02×1023=0.05mol,质量为0.05mol×30g/mol=1.5g,在标准状态下所占的体积约为0.05mol×22.4L/mol=1.12L,故答案为:1.5;1.12。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
药品 | NaNO2 (亚硝酸钠) |
性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目:________________。若有0.75mol 电子转移,则被还原的氧化剂粒子数为_______。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+ 而中毒,可服用维生素C 解毒。下列分析错误的是______(填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl 的是______ (填序号)。
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN 溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_______________。