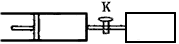题目内容
 如图所示,向A 和B 中都充入2mol X 和2mol Y,起始时VA=a L,VB=0.8a L,在相同温度和有催化剂的条件下,两容器中各自发生下列反应X(g)+Y(g)?2Z(g)+W(g) 达到平衡时,VA=1.3a L,(A容器活塞无摩擦,可自由滑动)则下列说法正确的是( )
如图所示,向A 和B 中都充入2mol X 和2mol Y,起始时VA=a L,VB=0.8a L,在相同温度和有催化剂的条件下,两容器中各自发生下列反应X(g)+Y(g)?2Z(g)+W(g) 达到平衡时,VA=1.3a L,(A容器活塞无摩擦,可自由滑动)则下列说法正确的是( )分析:根据图象知,A保持恒压,B保持恒容,
A、容器内气体的压强和容器体积以及气体的物质的量有关,符合方程PV=nRT;
B、打开K达新平衡等效为A中到达的平衡,根据X的转化率计算平衡后总的物质的量,再根据体积之比等于物质的量之比计算总体积,进而计算A容器的体积;
C、先根据相同条件下,气体的气体之比等于物质的量之比计算平衡后气体的物质的量,再结合方程式计算X反应的物质的量,最后根据转化率公式计算X的转化率,再结合B装置中压强对化学平衡的影响判断X的转化率;
D、打开K达新平衡等效为A中到达的平衡,根据X的转化率计算平衡后总的物质的量,再根据体积之比等于物质的量之比计算总体积,进而计算A容器的体积,升高温度,平衡向吸热方向移动,据此判断;
A、容器内气体的压强和容器体积以及气体的物质的量有关,符合方程PV=nRT;
B、打开K达新平衡等效为A中到达的平衡,根据X的转化率计算平衡后总的物质的量,再根据体积之比等于物质的量之比计算总体积,进而计算A容器的体积;
C、先根据相同条件下,气体的气体之比等于物质的量之比计算平衡后气体的物质的量,再结合方程式计算X反应的物质的量,最后根据转化率公式计算X的转化率,再结合B装置中压强对化学平衡的影响判断X的转化率;
D、打开K达新平衡等效为A中到达的平衡,根据X的转化率计算平衡后总的物质的量,再根据体积之比等于物质的量之比计算总体积,进而计算A容器的体积,升高温度,平衡向吸热方向移动,据此判断;
解答:解:A、根据公式PV=nRT,所以P=
,n相等,V越大,则P越小,起始时两容器中的压强A的较小,故A错误;
B、打开K达新平衡等效为A中到达的平衡,X的转化率为60%,参加反应的X的总的物质的量为4mol×60%=2.4mol,则:
X(g)+Y(g)?2Z(g)+W(g) 物质的量增多
1mol 1mol
2.4mol 2.4mol
平衡后容器中总物质的量8mol+2.4mol=10.4mol,气体的体积之比等于物质的量之比,高B容器温度,混合气体的温度升高,平衡向正反应方向移动,混合气体的总的物质的量增大,A容器体积会增大,故B正确;
C、达到平衡时,VA=1.3a L,等压、等温条件下,气体的体积之比等于气体的物质的量之比,所以平衡后混合气体的物质的量是2mol×1.3=2.6mol,设参加反应的A的物质的量为mmol,则:
X(g)+Y(g)?2Z(g)+W(g) 物质的量增多
1mol 1mol
mmol (2.6-2)mol
m=0.6,所以X物质的转化率=
=60%;B装置是在等容条件下,反应向正反应方向移动时,混合气体的物质的量增大,导致容器内气体压强增大,增大压强能抑制X的转化率,故B中X转化率小于A中X转化率,故C正确;
D、打开K达新平衡等效为A中到达的平衡,X的转化率为60%,参加反应的X的总的物质的量为4mol×60%=2.4mol,则:
X(g)+Y(g)?2Z(g)+W(g) 物质的量增多
1mol 1mol
2.4mol 2.4mol
平衡后容器中总物质的量8mol+2.4mol=10.4mol,气体的体积之比等于物质的量之比,AB两部分总体积是2.16aL,故D错误.
故选BC.
| nRT |
| V |
B、打开K达新平衡等效为A中到达的平衡,X的转化率为60%,参加反应的X的总的物质的量为4mol×60%=2.4mol,则:
X(g)+Y(g)?2Z(g)+W(g) 物质的量增多
1mol 1mol
2.4mol 2.4mol
平衡后容器中总物质的量8mol+2.4mol=10.4mol,气体的体积之比等于物质的量之比,高B容器温度,混合气体的温度升高,平衡向正反应方向移动,混合气体的总的物质的量增大,A容器体积会增大,故B正确;
C、达到平衡时,VA=1.3a L,等压、等温条件下,气体的体积之比等于气体的物质的量之比,所以平衡后混合气体的物质的量是2mol×1.3=2.6mol,设参加反应的A的物质的量为mmol,则:
X(g)+Y(g)?2Z(g)+W(g) 物质的量增多
1mol 1mol
mmol (2.6-2)mol
m=0.6,所以X物质的转化率=
| 0.6 |
| 1 |
D、打开K达新平衡等效为A中到达的平衡,X的转化率为60%,参加反应的X的总的物质的量为4mol×60%=2.4mol,则:
X(g)+Y(g)?2Z(g)+W(g) 物质的量增多
1mol 1mol
2.4mol 2.4mol
平衡后容器中总物质的量8mol+2.4mol=10.4mol,气体的体积之比等于物质的量之比,AB两部分总体积是2.16aL,故D错误.
故选BC.
点评:本题考查学生化学平衡的有关计算以及化学平衡移动的有关知识,注意打开K达新平衡等效为A中到达的平衡是解题关键,难度大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
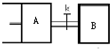 如图所示,向A中充入1mol X和1mol Y,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g)?2Z(g)+W(g)△H>0;达到平衡时,VA=1.2aL,则下列说法错误的是( )
如图所示,向A中充入1mol X和1mol Y,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g)?2Z(g)+W(g)△H>0;达到平衡时,VA=1.2aL,则下列说法错误的是( )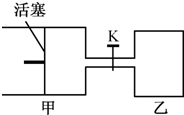 (2011?南京一模)如图所示,向甲和乙两容器中都充入2molX和2molY(K关闭) 起始V甲=0.8aL,V乙=aL,在相同恒定温度下,两容器中各自发生下列反应:X(g)+Y(g)═2Z(g)+W(g),达到平衡时,V甲=0.9aL,则下列说法错误的是( )
(2011?南京一模)如图所示,向甲和乙两容器中都充入2molX和2molY(K关闭) 起始V甲=0.8aL,V乙=aL,在相同恒定温度下,两容器中各自发生下列反应:X(g)+Y(g)═2Z(g)+W(g),达到平衡时,V甲=0.9aL,则下列说法错误的是( ) 2Z(g)+W(g) △H<0,达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g)+W(g) △H<0,达平衡时,A的体积为1.4aL。下列说法错误的是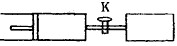
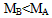
 2Z(g)+W(g) △H<0。达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g)+W(g) △H<0。达平衡时,A的体积为1.4aL。下列说法错误的是