题目内容
【题目】同温同压下,相同体积的CO和C2H4的比较中正确的是( ) ①所含的分子数目之比为1:1 ②所含的质子数目之比为1:1
③所含的原子总数目之比为1:3 ④两者的密度之比为:1:1.
A.①②③④
B.①②④
C.②③④
D.①③④
【答案】D
【解析】解:同温同压下,气体摩尔体积相同,则相同体积的CO和C2H4具有相同的物质的量,①根据n=nNA可知,二者所含的分子数相等,其分子数目之比为1:1,故①正确②所含的质子数目之比=质子物质的量之比=(1×14):(1×16)=7:8,故②错误;③CO和C2H4分子分别含有原子数为2、6,物质的量相等时含有的原子数之比=原子的物质的量之比=(1×2):(1×6)=1:3,故③正确;④二者摩尔质量相等,ρ= ![]() 可知两者的密度相等,其密度之比=1:1,故④正确;故选D.
可知两者的密度相等,其密度之比=1:1,故④正确;故选D.

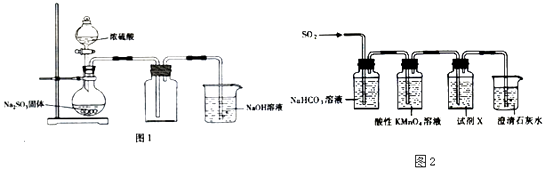
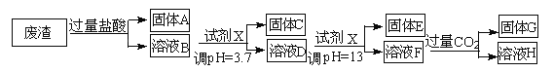
【题目】某硫酸工业废渣的主要成分为SiO2、MgO、Al2O3、Fe2O3等。回收废渣中金属元素的工艺流程如下:
已知常温条件下:
①阳离子以氢氧化物形式开始沉淀和恰好完全沉淀(阳离子浓度等于10-5mol·L-1 )时的pH 如下表所
示。
阳离子 | Fe3+ | Al3+ | Mg2+ |
开始沉淀时的pH | 1.9 | 3.7 | 9.6 |
恰好完全沉淀时的pH | 3.2 | 5.2 | 11.0 |
②饱和氨水溶液中c(OH-)约为1×10-3mol·L-1。
请回答下列问题:
(1)固体C为_________(填化学式)。
(2)上述流程中两次使用试剂X,试剂X是_________(填“氨水”或“氢氧化钠”),其理由是_________________。
(3)溶液D→固体E的过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是________________。
(4)写出溶液F→溶液H 的离子方程式:__________________。
(5)Ksp[Mg (OH )2]=_____________。