题目内容
【题目】现有一瓶FeCl3饱和溶液,写出其电离方程式: . 将FeCl3饱和溶液滴入沸水中,微热后,液体变为色,得到的是 .
【答案】FeCl3=Fe3++3Cl﹣;红褐色;Fe(OH)3(胶体)
【解析】解:氯化铁为 强电解质,完全电离产生三价铁离子和氢氧根离子,电离方程式:FeCl3=Fe3++3Cl﹣,
三价铁离子为弱碱阳离子,部分水解生成氢氧化铁胶体和氢离子,离子方程式:Fe3++3H2O Fe(OH)3(胶体)+3H+,溶液变为红褐色;
所以答案是:FeCl3=Fe3++3Cl﹣;红褐色;Fe(OH)3(胶体).

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】根据下列实验或实验操作和现象,所得结论正确的是:
选项 | 实验或实验操作 | 现象 | 实验结论 |
A | 用大理石和盐酸反应产生的气体立即通入一定浓度的Na2SiO3 溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
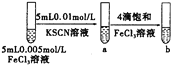
C |
| 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
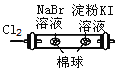
D |
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
A. A B. B C. C D. D