题目内容
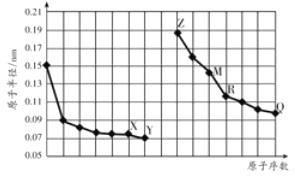
【题目】三元催化转化器能同时净化汽车尾气中的碳氢化合物(HC)、一氧化碳(CO)及氮氧化合物(NOx)三种污染物。催化剂选择铂铑合金,合金负载量不同时或不同的工艺制备的合金对汽车尾气处理的影响如图所示。下列说法正确的是
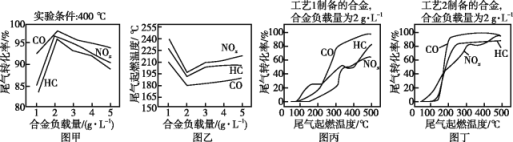
A.图甲表明,其他条件相同时,三种尾气的转化率随合金负载量的增大而增大
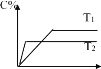
B.图乙表明,尾气的起燃温度随合金负载量的增大而降低
C.图甲和图乙表明,合金负载量越大催化剂活性越高
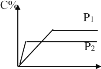
D.图丙和图丁表明,工艺2制得的合金的催化性能优于工艺1制得的合金
【答案】D
【解析】
A. 根据图甲所示可知:在400℃时,三种气体的转化率在合金负载量为2 g/L时最大,A错误;
B. 图乙表明,尾气的起燃温度在合金负载量为2 g/L时最低,其它各种合金负载量时起燃温度都比2 g/L时的高,B错误;
C. 图甲表示只有在合金负载量为2 g/L时尾气转化率最大,而图乙表示的是只有在合金负载量为2 g/L时尾气转化率最低,可见并不是合金负载量越大催化剂活性越高,C错误;
D. 图丙表示工艺1在合金负载量为2 g/L时,尾气转化率随尾气的起燃温度的升高而增大,而图丁表示工艺2在合金负载量为2 g/L时,尾气转化率在尾气的起燃温度为200℃时已经很高,且高于工艺1,因此制得的合金的催化性能:工艺2优于工艺1,D正确;
故合理选项是D。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】(1)“一氧化碳变换”是合成氨原料气生产中的重要环节,其反应方程式为:CO(g)+H2O(g)![]() CO2(g)+H2(g)。将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
CO2(g)+H2(g)。将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | CO2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 5 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 650 | 2 | 1 | A | B | t |
①实验1中从反应开始到达到平衡,以H2的浓度变化表示的反应速率为_________
②A=_________
③平衡常数:K(900℃)_________K(650℃)(填“>”、“<”或“=”).
(2)温度是一氧化碳变换中最重要的工艺条件,实际生产过程中将温度控制在400℃左右,可能的原因是__________。
(3)下列描述中能说明上述反应已达平衡的是___________________
a.v正(CO)=v逆(H2) b.气体的密度不随时间而变化
c.H2和CO2的比例保持不变 d.气体的压强不再发生变化
(4)C、H、O、N元素中,写出两两组合(不能重复)形成的非极性分子的电子式_________,极性分子的电子式_________。这四种元素形成的化合物_________(填“一定是”、“一定不是”、“不一定是”)离子化合物。