题目内容
【题目】铝氢化钠(NaAIH4)是有机合成的重要还原剂,其合成线路如下图所示。
已知AlCl3的熔点为190℃,沸点为178℃,在潮湿的空气中易水解。某实验小组利用下图中装置制备无水AlC13。
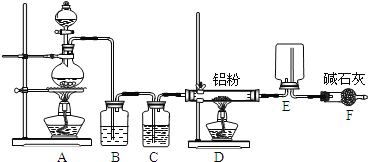
(1)①写出圆底烧瓶中发生反应的离子方程式______。
②装置F的作用是 ________。
(2)AlCl3与NaH反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的可能原因是 ________。
(3)利用铝氢化钠遇水反应生成的氢气的体积测定铝氢化钠样品纯度。
①其反应的化学方程式为 ______ 。
②设计如下四种装置测定铝氢化钠样品的纯度(杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是 ______(填编号)。
【答案】 ![]() 吸收未反应的Cl2,并防止空气中的水蒸气进入装置B NaH是离子化合物,难溶于有机溶剂,使反应物难以接触
吸收未反应的Cl2,并防止空气中的水蒸气进入装置B NaH是离子化合物,难溶于有机溶剂,使反应物难以接触 ![]() 乙
乙
【解析】(1)①由制取Cl2的化学方程式:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,可知离子方程式为MnO2+4H++2Cl-
MnCl2+Cl2↑+2H2O,可知离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;②氯气有毒,会污染空气,能与碱反应,利用装置F可吸收未反应的Cl2,并防止空气中的水蒸气进入装置B;(2) NaH是离子化合物,难溶于有机溶剂,使反应物难以接触,AlCl3与NaH反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,否则NaH的转化率较低;(3) ①铝氢化钠遇水反应生成的氢气和偏铝酸钠,其反应的化学方程式为NaAlH4+2H2O=NaAlO2+4H2↑;②测定铝氢化钠的纯度,就是利用其与水反应生成氢气,测定氢气的体积,所以给的装置中乙的装置可以较准确的测定氢气的体积,所以选择乙。甲中锥形瓶中的压强变大,可能液体不能顺利流下,铝氢化钠或许不能完全反应,丙装置中导管中可能有水,使测定的气体的体积不准确,丁的操作中氢气的体积不好读数。读取气体体积时要冷却到室温,标志是连续两次读数的氢气体积相等。
Mn2++Cl2↑+2H2O;②氯气有毒,会污染空气,能与碱反应,利用装置F可吸收未反应的Cl2,并防止空气中的水蒸气进入装置B;(2) NaH是离子化合物,难溶于有机溶剂,使反应物难以接触,AlCl3与NaH反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,否则NaH的转化率较低;(3) ①铝氢化钠遇水反应生成的氢气和偏铝酸钠,其反应的化学方程式为NaAlH4+2H2O=NaAlO2+4H2↑;②测定铝氢化钠的纯度,就是利用其与水反应生成氢气,测定氢气的体积,所以给的装置中乙的装置可以较准确的测定氢气的体积,所以选择乙。甲中锥形瓶中的压强变大,可能液体不能顺利流下,铝氢化钠或许不能完全反应,丙装置中导管中可能有水,使测定的气体的体积不准确,丁的操作中氢气的体积不好读数。读取气体体积时要冷却到室温,标志是连续两次读数的氢气体积相等。

【题目】下列除去杂质(括号内的物质是杂质)时,选用的试剂或方法正确的是( )
A | B | C | D | |
试样 | NaCl溶液(Na2CO3) | NH4Cl固体(I2) | CO2(SO2) | NaBr溶液(Br2) |
除杂试剂 | 澄清石灰水 | 加热 | NaOH溶液 | 用CCl4萃取、 |
A.A
B.B
C.C
D.D
【题目】现有部分元素的性质或原子结构信息如表,据此回答下列问题:
元素编号 | 元素性质或原子结构 |
T | M层上有2对成对电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物的水溶液显碱性 |
Z | 短周期元素最高正化合价是+7价 |
W | 3d能级电子数是最外层电子数的3倍 |
(1)元素X的基态原子核外共有________种空间运动状态不同的电子,元素X与H元素形成的化合物是当今重要的能源,该化合物的电子式为________。
(2)元素Y的价电子排布图为________________,元素Y与元素T相比,电负性较大的是________(用元素符号表示)。
(3)元素Z与元素T相比,非金属性强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为________,稳定性比较:W3+________W2+(填“>”或“<”),原因是__________________________________________________________________________。