题目内容
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”,“中性”或“碱性”,下同).
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液,溶液中c(Na+) c(CH3COO-)(填“>”、“=”或“<”下同)
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 .
(4)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则原醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n.
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液,溶液中c(Na+)
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈
(4)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则原醋酸溶液中c(H+)
考点:酸碱混合时的定性判断及有关ph的计算,pH的简单计算
专题:电离平衡与溶液的pH专题
分析:(1)醋酸为弱酸,将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,恰好生成醋酸钠,为强碱弱酸盐,溶液呈碱性;
(2)pH=3的醋酸和pH=11的氢氧化钠溶液,醋酸浓度较大,等体积混合时,醋酸过量;
(3)根据溶液中电荷守恒及醋酸根离子与钠离子浓度相等进行判断氢离子与氢氧根离子浓度关系;
(4)醋酸为弱电解质,溶液中部分电离出氢离子,等体积的两溶液混合pH=7,若m=n,溶液显示中性,则醋酸浓度稍大.
(2)pH=3的醋酸和pH=11的氢氧化钠溶液,醋酸浓度较大,等体积混合时,醋酸过量;
(3)根据溶液中电荷守恒及醋酸根离子与钠离子浓度相等进行判断氢离子与氢氧根离子浓度关系;
(4)醋酸为弱电解质,溶液中部分电离出氢离子,等体积的两溶液混合pH=7,若m=n,溶液显示中性,则醋酸浓度稍大.
解答:
解:(1)醋酸为弱电解质,将等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合后,恰好生成CH3COONa,为强碱弱酸盐,
故答案为:碱性;
(2)醋酸为弱电解质,pH=3的醋酸溶液中氢离子浓度为0.001mol/L,醋酸的浓度大于0.001mol/L,而pH=11的氢氧化钠溶液的浓度为0.001mol/L,两溶液等体积混合后醋酸过量,溶液呈酸性,则c(H+)>c(OH-),溶液中存在电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),则c(Na+)<c(CH3COO-),
故答案为:<;
(3)将物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中存在电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),溶液中醋酸根离子和钠离子浓度相等,则氢离子与氢氧根离子浓度相等,所以溶液呈中性,
故答案为:中性;
(4)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,当m=n时,两溶液恰好反应生成醋酸钠,溶液显示碱性,若使溶液的pH=7,则醋酸的浓度应该稍大一些,即m>n;由于醋酸为弱酸,则溶液中氢离子浓度小于氢氧化钠溶液中氢氧根离子浓度,即c(H+)<氢氧化钠溶液中c(OH-),
故答案为:<;>.
故答案为:碱性;
(2)醋酸为弱电解质,pH=3的醋酸溶液中氢离子浓度为0.001mol/L,醋酸的浓度大于0.001mol/L,而pH=11的氢氧化钠溶液的浓度为0.001mol/L,两溶液等体积混合后醋酸过量,溶液呈酸性,则c(H+)>c(OH-),溶液中存在电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),则c(Na+)<c(CH3COO-),
故答案为:<;
(3)将物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中存在电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),溶液中醋酸根离子和钠离子浓度相等,则氢离子与氢氧根离子浓度相等,所以溶液呈中性,
故答案为:中性;
(4)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,当m=n时,两溶液恰好反应生成醋酸钠,溶液显示碱性,若使溶液的pH=7,则醋酸的浓度应该稍大一些,即m>n;由于醋酸为弱酸,则溶液中氢离子浓度小于氢氧化钠溶液中氢氧根离子浓度,即c(H+)<氢氧化钠溶液中c(OH-),
故答案为:<;>.
点评:本题考查酸碱混合以及溶液pH的大小比较,为高考常见题型,题目难度中等,本题注意从溶液电中性的角度比较溶液离子浓度的大小关系,另外把握盐类水解的原理及其应用方法.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
常温下,在0.005mol/L H2SO4中,水的离子积是( )
| A、1×10-14 |
| B、1×10-12 |
| C、1×10-24 |
| D、1×10-4 |
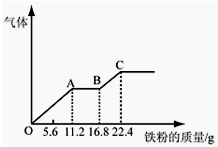 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A、原混合酸中NO3-物质的量浓度为2mol/L |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为2.5mol?L-1 |
下列有关离子键、共价键的叙述中正确的是( )
| A、离子化合物中只存在离子键,没有共价键 |
| B、构成单质分子的粒子中一定含有共价键 |
| C、共价化合物分子中一定不存在离子键 |
| D、仅由非金属元素组成的化合物中一定不含离子键 |
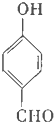 对基苯甲醛,…俗称PHBA,是-种重要的有机化工原料.其结构如图所示
对基苯甲醛,…俗称PHBA,是-种重要的有机化工原料.其结构如图所示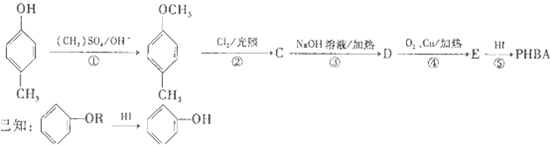
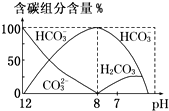 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.
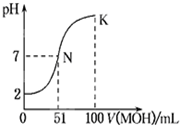 常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题: