题目内容
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
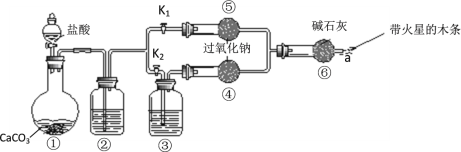
(装置分析)
(1)装置①中反应的离子方程式是___________;
(2)装置②中的试剂是______(填字母),装置③中的试剂是_________(填字母);
a 饱和NaHCO3溶液 b 饱和Na2CO3溶液 c 浓H2SO4 d NaOH溶液
(进行实验)
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
步骤1中_____________,步骤2中_____________;
(4)步骤2中过氧化钠跟二氧化碳反应的化学方程式是_______________;
(实验反思)
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应” 。其理由是____________;
(6)需要补充的实验操作是:取⑤中反应后的少量固体,______________;
(测定实验)测定反应后⑤中固体CO32-的质量分数
(7)将反应后⑤中固体,称量质量为ag。将ag固体溶于水,加入__________(填“BaCl2”或“CaCl2”)溶液,与未选物质相比的优点是___________。将生成的沉淀过滤、洗涤、干燥、称量,得固体质量为bg,计算质量分数。
【答案】CaCO3+2H+= Ca2++H2O+CO2↑ a c 步骤1中木条不复燃 步骤2中木条复燃 ![]() 气体中有水,水也可与Na2O2反应产生O2使木条复燃 加入稀盐酸,将产生的气体通入澄清的石灰水中【或加BaCl2溶液等体现检验CO32-的方法即可,加CaCl2不给分】 BaCl2 生成沉淀质量更大,相对误差更小【或加CaCl2会产生微溶的Ca(OH)2】
气体中有水,水也可与Na2O2反应产生O2使木条复燃 加入稀盐酸,将产生的气体通入澄清的石灰水中【或加BaCl2溶液等体现检验CO32-的方法即可,加CaCl2不给分】 BaCl2 生成沉淀质量更大,相对误差更小【或加CaCl2会产生微溶的Ca(OH)2】
【解析】
将碳酸钙和稀盐酸反应生成二氧化碳、氯化钙和水,先除掉二氧化碳中的HCl气体,一部分气体直接通入过氧化钠,另一部分先干燥再通入过氧化钠中,验证有无氧气;但也有可能是过氧化钠和水在反应,因此要验证产物中是否生成了碳酸根,常用氯化钡来验证。
⑴装置①中反应的离子方程式是CaCO3+2H+ = Ca2++H2O+CO2↑;故答案为:CaCO3+2H+= Ca2++H2O+CO2↑。
⑵装置②中的试剂主要是除掉HCl,因此用a,装置③中的试剂主要干燥二氧化碳气体,因此用c;故答案为:a;c。
⑶步骤1中没有氧气生成,因此木条不复燃,步骤2中产生了氧气,因此使木条复燃;故答案为:木条不复燃;木条复燃。
⑷步骤2中过氧化钠跟二氧化碳反应的化学方程式是2Na2O2+2CO2 ![]() 2Na2CO3+O2↑;故答案为:2Na2O2+2CO2
2Na2CO3+O2↑;故答案为:2Na2O2+2CO2 ![]() 2Na2CO3+O2↑。
2Na2CO3+O2↑。
⑸有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应” 。其理由是气体中有水,水也可与Na2O2反应产生O2使木条复燃;故答案为:气体中有水,水也可与Na2O2反应产生O2使木条复燃。
⑹需要补充的实验主要是验证有碳酸钠生成,通过反应生成二氧化碳来验证,因此操作是:取⑤中反应后的少量固体加入稀盐酸,将产生的气体通入澄清的石灰水中[或加BaCl2溶液等体现检验CO32-的方法即可,加CaCl2不给分];故答案为:加入稀盐酸,将产生的气体通入澄清的石灰水中[或加BaCl2溶液等体现检验CO32-的方法即可,加CaCl2不给分]。
⑺将反应后⑤中固体,称量质量为ag。将ag固体溶于水,加入BaCl2溶液,生成碳酸钡沉淀,与氯化钙反应生成碳酸钙和氢氧化钙,因此与未选物质相比的优点是生成沉淀质量更大,相对误差更小[或加CaCl2会产生微溶的Ca(OH)2];故答案为:BaCl2溶液;生成沉淀质量更大,相对误差更小[或加CaCl2会产生微溶的Ca(OH)2]。