题目内容
【题目】写出下列反应的化学方程式:
①乙炔与足量溴水 .
②C6H5﹣OH与浓溴水  .
.
③CH3CH2CHO和新制Cu(OH)2的反应 .
【答案】①CH≡CH+2Br2→CHBr2CHBr2;
②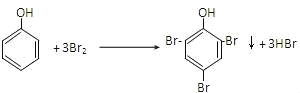 ;
;
③CH3CH2CHO+2Cu(OH)2、![]() 2H2O+Cu2O↓+CH3CH2COOH.
2H2O+Cu2O↓+CH3CH2COOH.
【解析】
试题分析:①乙炔与足量溴水反应,溴水褪色,生成1,1,2,2﹣四溴乙烷;
②苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于取代;
③CH3CH2CHO和新制Cu(OH)2的反应生成丙酸、氧化亚铜、水.
解:①乙炔能够和溴水发生加成反应,按1:2加成,生成1,1,2,2﹣四溴乙烷,反应的化学方程式为:CH≡CH+2Br2→CHBr2CHBr2,
故答案为:CH≡CH+2Br2→CHBr2CHBr2;
②苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于发生取代反应,反应的化学方程式为: ,
,
故答案为: ;
;
③丙醛与新制的氢氧化铜反应,醛基被氧化,生成丙酸和氧化亚铜、水,反应为:CH3CH2CHO+2Cu(OH)2、![]() 2H2O+Cu2O↓+CH3CH2COOH,
2H2O+Cu2O↓+CH3CH2COOH,
故答案为:CH3CH2CHO+2Cu(OH)2、![]() 2H2O+Cu2O↓+CH3CH2COOH.
2H2O+Cu2O↓+CH3CH2COOH.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
【题目】为探究影响化学反应速率的影响因素,将等质量的铁与过量盐酸反应,其他实验条件见下表。其中铁被反应完消耗时间最少的组别是
组别 | c(HCl)/ mol·L-1 | 温度/℃ | 铁的状态 |
A | 2.0 | 25 | 块状 |
B | 2.5 | 30 | 粉末状 |
C | 2.5 | 50 | 块状 |
D | 2.5 | 50 | 粉末状 |
A. A B. B C. C D. D

