题目内容
【题目】A、B、C、D、E为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成A2C和A2C2两种常见的液态化合物.请回答下列问题:
(1)D在周期表中的位置 ,E的简单阴离子结构示意图 ,A2C2的结构式:
(2)C、D、E三种元素简单离子的离子半径由大到小的顺序是 。
(3)请举一个事实说明C和E的非金属性强弱:
(4)用含A元素最简单的有机化合物与炽热的氧化铜反应生成一种单质、液态氧化物和一种可以使澄清石灰水变浑浊的气体,其化学方程式为 .
【答案】⑴第三周期IA族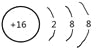 H-O-O-H
H-O-O-H
⑵S2-﹥O2-﹥Na+
⑶水蒸气的稳定性比H2S强,说明O的非金属性比S强
⑷CH4+4CuO=4Cu+2H2O+CO2
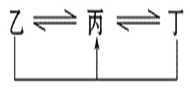
【解析】试题分析:A、B、C、D、E为原子序数依次增大的五种短周期元素,A单质试自然界中密度最小的气体,则A为H元素;B、C和E在周期表中相邻,且C、E同主族,所以B、C、E在周期表中的位置关系为![]() ,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,则D为Na;B、C的最外层电子数之和等于D的原子核外电子数,则B、C最外层电子数分别为5、6,故B为N元素,C为O元素,E为S元素,A和C可形成化合物H2O、H2O2,
,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,则D为Na;B、C的最外层电子数之和等于D的原子核外电子数,则B、C最外层电子数分别为5、6,故B为N元素,C为O元素,E为S元素,A和C可形成化合物H2O、H2O2,
(1)由上述分析可知,D为Na,在周期表中的位置:第三周期IA族,E的离子结构示意图为![]() ,A2C2为过氧化氢,结构式为H-O-O-H,
,A2C2为过氧化氢,结构式为H-O-O-H,
故答案为:第三周期IA族;![]() ;H-O-O-H;
;H-O-O-H;
(2)电子层数越多半径一般越大,相同电子层数,原子序数越小半径越大,故离子半径大小顺序为S2->O2->Na+,故答案为:S2->O2->Na+;
(3)气态氢化物越稳定,元素非金属性越强,水蒸气的稳定性比H2S强,说明O的非金属性比S强,
故答案为:水蒸气的稳定性比H2S强,说明O的非金属性比S强;
(4)A元素最简单的有机化合物为甲烷,与炽热的氧化铜反应生成一种单质、液态氧化物和一种可以使澄清石灰水变浑浊的气体,其化学方程式为CH4+4CuO=4Cu+2H2O+CO2,
故答案为:CH4+4CuO=4Cu+2H2O+CO2.

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】如图所示,X、Y分别是直流电源的两极,通电后发生a极板质量增加,b极板处有无色无臭气体放出。符合这一情况的是( )
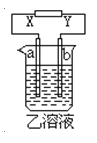
a极板 | b极板 | X电极 | 乙溶液 | |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |