题目内容
IA族碱金属与VⅡA族元素所形成的化合物大都具有的性质是( )
①高沸点 ②能溶于水 ③水溶液能导电 ④低熔点 ⑤熔融状态不导电.
①高沸点 ②能溶于水 ③水溶液能导电 ④低熔点 ⑤熔融状态不导电.
| A、①②③ | B、③④⑤ |
| C、①④⑤ | D、②③⑤ |
考点:原子结构与元素的性质,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:IA族碱金属与VⅡA族元素所形成的化合物为可溶性离子化合物,且为强电解质,第IA族碱金属卤化物具有高沸点、可溶的特点,含有自由移动离子的物质能导电.
解答:
解:IA族碱金属与VⅡA族元素所形成的化合物为可溶性离子化合物,且为强电解质,具有高沸点特点,能溶于水,在水分子的作用下电离出阴阳离子而使其溶液导电,熔融状态导电,
故选A.
故选A.
点评:本题考查了碱金属卤化物的性质,碱金属卤化物都易溶于水,注意电解质和溶液导电的关系,为易错点.

练习册系列答案
相关题目
下列粒子(或化学键)的数目之比不是1:1的是( )
| A、氘原子(2H)中的质子和中子 |
| B、碳酸氢钠溶液中的阴离子和阳离子 |
| C、CO2分子中的σ键和π键 |
| D、常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH- |
下列离子方程式对应的化学方程式正确的是( )
| A、H++OH-═H2O CH3COOH+NaOH═CH3COONa+H2O |
| B、Ba2++SO42-═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O |
| C、CO32-+2H+═CO2↑+H2O CaCO3+2HCl═CaCl2+CO2↑+H2O |
| D、3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O |
关于键长、键能和键角,下列说法不正确的是( )
| A、键长大小与两成键原子之间的共用电子对数目有关 |
| B、键角与共价键的方向性有关 |
| C、键能越大,键长越长,共价化合物越稳定 |
| D、键角大小并不决定键长、键能的大小 |
下列说法正确的是( )
| A、MgSO4晶体中只存在离子键 |
| B、含有共价键的化合物一定是共价化合物 |
| C、酸性:HNO3>H2CO3>H2SiO3 |
| D、普通钠玻璃成分可表示为Na2O?CaO?6SiO2,有固定的熔点 |
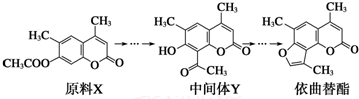
依曲替酯是一种皮肤病用药,它可以由原料X经过多步反应合成.
下列说法不正确的是( )

下列说法不正确的是( )
| A、原料X与中间体Y互为同分异构体 |
| B、原料X可以使酸性KMnO4溶液褪色 |
| C、中间体Y能发生加成、取代、消去、氧化、还原反应 |
| D、1mol依曲替酯能与2mol NaOH发生反应 |