题目内容
【题目】下列化学反应的离子方程式正确的是( )
A. 用小苏打治疗胃酸过多:HCO3-+H+===CO2↑+H2O
B. 往碳酸镁中滴加稀盐酸:CO32-+2H+===CO2↑+H2O
C. 往澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2===CaCO3↓+H2O
D. 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-===BaSO4↓+H2O
【答案】A
【解析】
试题A、小苏打是碳酸氢钠,治疗胃酸过多时反应生成二氧化碳和水,HCO![]() +H+=CO2↑+H2O,故A正确;B、碳酸镁不溶于水,用化学式表示,故B错误;C、往澄清石灰水中通入过量二氧化碳生成碳酸氢钙,没有碳酸钙沉淀生成,故C错误;D、氢氧化钡是二元强碱,稀硫酸是二元强离子方程式为Ba2++SO
+H+=CO2↑+H2O,故A正确;B、碳酸镁不溶于水,用化学式表示,故B错误;C、往澄清石灰水中通入过量二氧化碳生成碳酸氢钙,没有碳酸钙沉淀生成,故C错误;D、氢氧化钡是二元强碱,稀硫酸是二元强离子方程式为Ba2++SO![]() +2H++2OH-=BaSO4↓+2H2O,故D错误;故选A。
+2H++2OH-=BaSO4↓+2H2O,故D错误;故选A。

【题目】三氯乙醛是基本有机合成原料之一,是生产农药、医药的重要中间体。某化学兴趣小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。
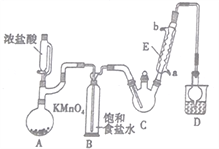
查阅资料,有关信息如下:
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O、CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)仪器E的名称是____________,冷凝水的流向是________进_______出(填“a”或“b”)。
(2)该设计流程中存在一处缺陷,该缺陷是__________,引起的后果是_________________。
(3)仪器A中发生反应的离子方程式为____________________。
(4)该装置C可采用_______________,加热的方法以控制反应温度在70℃左右。
(5)装置D干燥管的作用为_______________,装置D烧杯中的试剂是_______________。
(6)反应结束后,从C中的混合物中分离出Cl3CCOOH的方法是____________(填名称)。
(7)已知:常温下Ka(CCl3COOH)=1.0×10-1mol·L-1,Ka(CH3COOH)=1.7×10-5mol·L-1,请设计实验证明三氯乙酸、乙酸的酸性强弱:____________________________。