题目内容
【题目】科学家最新研制的利用氯化氢和氢气生产高纯硅的工艺流程如图所示:
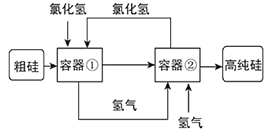
容器①中的反应为:Si(粗)+3HCl(g)=SiHCl3(l)+H2(g);容器②中进行的反应为:SiHCl3+H2=Si(纯)+3HCl,下列说法正确的是
A.反应①和②中HCl均作为氧化剂
B.该工艺流程的优点是部分反应物可循环使用
C.最好用分液的方法分离Si和SiHCl3
D.由反应①可知Si可与盐酸发生反应
【答案】B
【解析】
从流程图中可以看出,容器①中,Si(粗)与HCl(g)反应,生成SiHCl3(l)和H2(g);容器②中,SiHCl3(l)与H2(g)反应,生成Si(纯)和HCl(g);HCl(g)和H2(g)可以循环使用。
A.反应①中HCl作氧化剂,反应②中HCl是氧化产物,A不正确;
B.在该工艺流程中,HCl(g)和H2(g)可以循环使用,B正确;
C.Si固体和SiHCl3液体应使用过滤法分离,C不正确;
D.反应①中,Si与氯化氢在高温条件下发生反应,而不是与盐酸反应,D不正确;
故选B。

练习册系列答案
相关题目