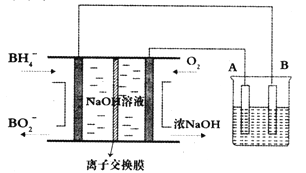
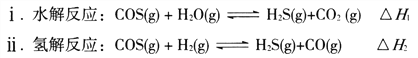��Ŀ����
����Ŀ�����Ҷ���(PEG) ��һ����;�㷺�ľۺ��1,2-�Ҷ���̼����(�ֳ�Ϊ̼��������) ��һ��ҽҩ�м��塣ijС������A Ϊԭ�Ϻϳ�PEG��̼����������·�����������
��֪: 2C2H5OH+CO+1/2O2 ![]() C2H5OCOOC2H5+H2O
C2H5OCOOC2H5+H2O
�ش�����������
��1��A������Ϊ____________�� A��B�ķ�Ӧ����Ϊ__________��C �ĺ˴Ź��������з������Ϊ___________��F�ķ���ʽΪ____________________��
��2��B��C�Ļ�ѧ����ʽΪ____________��
��3��C��һ�������·����ۺϷ�Ӧ����PEC����ѧ����ʽΪ___________________����ij��PEG��ƽ����Է�������Ϊ2000�� ����ƽ���ۺ϶�Ϊ____________________��
��4��E��ͬ���칹���У�������OCOO�����ŵĹ���___��(������E�������칹)��
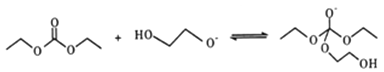
��5��������ΪC��E����F�ķ�Ӧ���̿�������:
��HOCH2CH2OH + CO32-![]() HOCH2CH2O-+HCO3-
HOCH2CH2O-+HCO3-
��
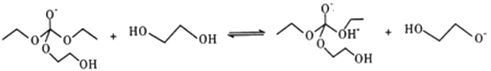
��
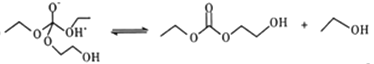
��
��
�ޢߢ��
��HOCH2CH2O- +HCO3-��HOCH2CH2OH+CO32-
д�������������ޢߢ��ķ�Ӧ����ʽ___________________��
���𰸡� ��ϩ �ӳɷ�Ӧ 1:2 C3H4O3 BrCH2CH2Br + 2NaOH![]() HOCH2CH2OH + 2NaBr n HOCH2CH2OH
HOCH2CH2OH + 2NaBr n HOCH2CH2OH ![]() HO
HO![]() CH2CH2O
CH2CH2O![]() H +��n -1��H2O 45.0 6
H +��n -1��H2O 45.0 6 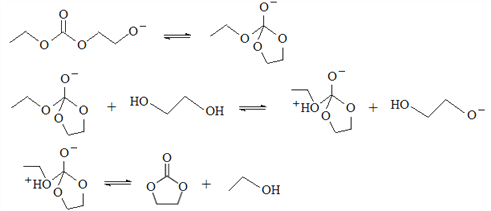
����������������ͼ��CΪHOCH2CH2OH��B����������ˮ��Һ��ˮ������C����BΪ±������BΪBrCH2CH2Br����AΪ��ϩ��CH2=CH2������ϩ��ˮ�ӳ�����D��DΪ�Ҵ���CH3CH2OH����������Ϣ��2C2H5OH+CO+1/2O2![]() C2H5OCOOC2H5+H2O����DΪC2H5OCOOC2H5��C�����ۺϷ�Ӧ���ɾ��Ҷ���(PEG)��C��E��̼��ش��������¼��뷴Ӧ����̼����������
C2H5OCOOC2H5+H2O����DΪC2H5OCOOC2H5��C�����ۺϷ�Ӧ���ɾ��Ҷ���(PEG)��C��E��̼��ش��������¼��뷴Ӧ����̼����������
��1����������������AΪ��ϩ��A��B����ϩ����ļӳɷ�Ӧ��C�к���2�ֻ�������ԭ�ӣ��ʺ˴Ź��������з������Ϊ2:4=1:2��F�ķ���ʽΪC3H4O3���ʴ�Ϊ����ϩ���ӳɷ�Ӧ��1:2��C3H4O3��
��2��B��C��±������ˮ�ⷴӦ����Ӧ�Ļ�ѧ����ʽΪBrCH2CH2Br + 2NaOH![]() HOCH2CH2OH + 2NaBr���ʴ�Ϊ��BrCH2CH2Br + 2NaOH
HOCH2CH2OH + 2NaBr���ʴ�Ϊ��BrCH2CH2Br + 2NaOH![]() HOCH2CH2OH + 2NaBr��
HOCH2CH2OH + 2NaBr��
��3���Ҷ�����һ�������·����ۺϷ�Ӧ����PEC����Ӧ�Ļ�ѧ����ʽΪn HOCH2CH2OH ![]() HO
HO![]() CH2CH2O
CH2CH2O![]() H +��n -1��H2O����ij��PEG��ƽ����Է�������Ϊ2000������ƽ���ۺ϶�=
H +��n -1��H2O����ij��PEG��ƽ����Է�������Ϊ2000������ƽ���ۺ϶�=![]() =45.0���ʴ�Ϊ��n HOCH2CH2OH
=45.0���ʴ�Ϊ��n HOCH2CH2OH ![]() HO
HO![]() CH2CH2O
CH2CH2O![]() H +��n -1��H2O�� 45.0��
H +��n -1��H2O�� 45.0��
��4��EΪC2H5OCOOC2H5������ͬ���칹���У�������OCOO�����ŵĹ���HOCOO CH
��5������C��E����F�ķ�Ӧ��������HOCH2CH2OH+CO32-![]() HOCH2CH2O-+HCO3-����
HOCH2CH2O-+HCO3-����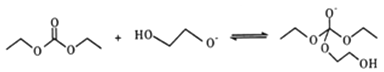 ����
����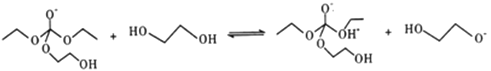 ����
����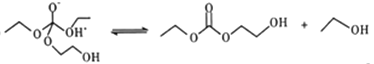 ����
���� �����Т���ٵķ�Ӧԭ�����ƣ����Ӧ����ڵ�ԭ�����ƣ�������ղ���
�����Т���ٵķ�Ӧԭ�����ƣ����Ӧ����ڵ�ԭ�����ƣ�������ղ���![]() �Ľṹ����Ϊ
�Ľṹ����Ϊ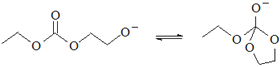 ����
����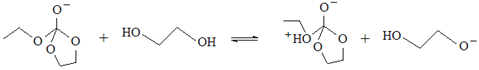 ����
����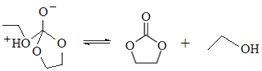 ����HOCH2CH2O-+HCO3-��HOCH2CH2OH+CO32-���ʴ�Ϊ����
����HOCH2CH2O-+HCO3-��HOCH2CH2OH+CO32-���ʴ�Ϊ���� ����
����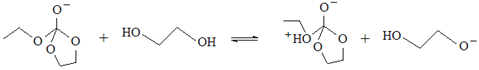 ����
���� ��
��