��Ŀ����
��14�֣�ij�о���ѧϰС����������ѧ֪ʶ�Ʊ����ᴿ����ͭ������ԭ��Ϊ�Ͼ�ͭ�ģ�����Լ2%���������ʺ��Բ��ƣ����������£�
I���Ʊ�����ͭ
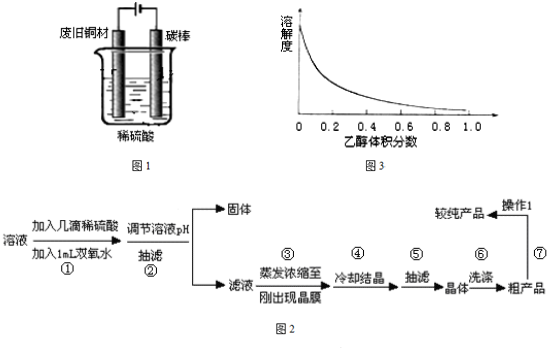
װ����ͼ��д�����������ĵ缫��Ӧʽ �� ��
II���ᴿ����ͭ
����Ӧ������ȡ���缫���������������ᴿ�õ�����ͭ���壨CuSO4��5H2O��
��֪����Һ��Fe2+��Fe3+��Cu2+�γ����������pH���±�
|
���� |
��ʼ������pH |
��ȫ������pH |
|
Fe2+ |
6.4 |
8.4 |
|
Fe3+ |
2.4 |
3.1 |
|
Cu2+ |
5.2 |
6.5 |
��1��д������ٷ�����Ӧ�����ӷ���ʽ ��
��2��������пɼ��� ���ѧʽ��������ҺpH�� ���Χ����
��3������۲������ɵ�ԭ���� ��
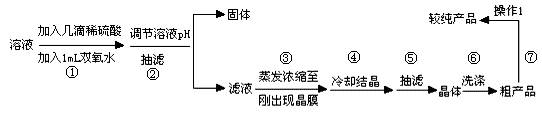
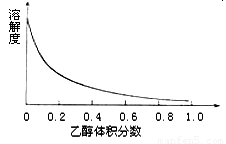
��4����ͼ��ʾ����ͭ�������Ҵ�ˮ����ܼ����ܽ�����Ҵ���������ı仯���ߣ������ʺ���Ϊ�����ϴ��Һ�� ��
A����ˮ�Ҵ� B������ˮ
C��95%�Ҵ���Һ D��������������Һ
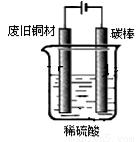
��5������1�������� ��
(14��) I�� Fe-2e-=Fe2+ ��1�֣� �� Cu-2e-=Cu2+ ��1�֣�
II����1��2Fe2++2H++H2O2=2Fe3++2H2O��2�֣�
��2��CuO��CuCO3��Cu2(OH)2CO3(��дһ�֣���2�֣�
3.1��5.2��ֻҪ����������ڵĶ����֣���2�֣�
��3����ֹ����ͭ����ʧȥ�ᾧˮ��2�֣� ��4��C ��2�֣� ��5���ؽᾧ��2�֣�
��������

��14�֣�ij�о���ѧϰС����������ѧ֪ʶ�Ʊ����ᴿ����ͭ������ԭ��Ϊ�Ͼ�ͭ�ģ�����Լ2%���������ʺ��Բ��ƣ����������£�
I���Ʊ�����ͭ
װ����ͼ��д�����������ĵ缫��Ӧʽ �� ��
II���ᴿ����ͭ
����Ӧ������ȡ���缫���������������ᴿ�õ�����ͭ���壨CuSO4��5H2O��
��֪����Һ��Fe2+��Fe3+��Cu2+�γ����������pH���±�
| ���� | ��ʼ������pH | ��ȫ������pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.4 | 3.1 |
| Cu2+ | 5.2 | 6.5 |
��1��д������ٷ�����Ӧ�����ӷ���ʽ ��
��2��������пɼ��� ���ѧʽ��������ҺpH�� ���Χ����
��3������۲������ɵ�ԭ���� ��
��4����ͼ��ʾ����ͭ�������Ҵ�ˮ����ܼ����ܽ�����Ҵ���������ı仯���ߣ������ʺ���Ϊ�����ϴ��Һ�� ��
A����ˮ�Ҵ� B������ˮ
C��95%�Ҵ���Һ D��������������Һ
��5������1�������� ��
��14�֣�ij�о���ѧϰС����������ѧ֪ʶ�Ʊ����ᴿ����ͭ������ԭ��Ϊ�Ͼ�ͭ�ģ�����Լ2%���������ʺ��Բ��ƣ����������£�
I���Ʊ�����ͭ
װ����ͼ��д�����������ĵ缫��Ӧʽ �� ��
II���ᴿ����ͭ
����Ӧ������ȡ���缫���������������ᴿ�õ�����ͭ���壨CuSO4��5H2O��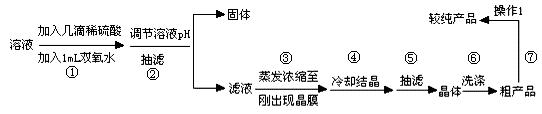
��֪����Һ��Fe2+��Fe3+��Cu2+�γ����������pH���±�
| ���� | ��ʼ������pH | ��ȫ������pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.4 | 3.1 |
| Cu2+ | 5.2 | 6.5 |
��2��������пɼ��� ���ѧʽ��������ҺpH�� ���Χ����
��3������۲������ɵ�ԭ���� ��
��4����ͼ��ʾ����ͭ�������Ҵ�ˮ����ܼ����ܽ�����Ҵ���������ı仯���ߣ������ʺ���Ϊ�����ϴ��Һ�� ��
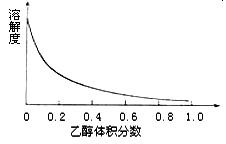
| A����ˮ�Ҵ� | B������ˮ |
| C��95%�Ҵ���Һ | D��������������Һ |
��14�֣�ij�о���ѧϰС����������ѧ֪ʶ�Ʊ����ᴿ����ͭ������ԭ��Ϊ�Ͼ�ͭ�ģ�����Լ2%���������ʺ��Բ��ƣ����������£�
I���Ʊ�����ͭ
װ������ͼ��д�����������ĵ缫��Ӧʽ �� ��
�� ��
II���ᴿ����ͭ
����Ӧ������ȡ���缫���������������ᴿ�õ�����ͭ���壨CuSO4��5H2O��

��֪����Һ��Fe2+��Fe3+��Cu2+�γ����������pH���±�
|
���� |
��ʼ������pH |
��ȫ������pH |
|
Fe2+ |
6.4 |
8.4 |
|
Fe3+ |
2.4 |
3.1 |
|
Cu2+ |
5.2 |
6.5 |
��1��д������ٷ�����Ӧ�����ӷ���ʽ �� ��
��2��������пɼ��� �� ���ѧʽ��������ҺpH�� �� ���Χ����
��3������۲������ɵ�ԭ���� �� ��

��4����ͼ��ʾ����ͭ�������Ҵ�ˮ����ܼ����ܽ�����Ҵ���������ı仯���ߣ������ʺ���Ϊ�����ϴ��Һ�� �� ��
A����ˮ�Ҵ� B������ˮ
C��95%�Ҵ���Һ D��������������Һ
��5������1�������� �� ��