题目内容
钛由于具有密度小、强度高、耐高温、抗腐蚀性强等优点,在现代科学技术上有着广泛的用途。工业上常用钛铁矿(主要成分为FeTiO3,同时含有铁的氧化物)为原料,经过一系列反应来制得钛,其流程大致如下。其中反应②目的是使Ti4+与水作用生成Ti(OH)4沉淀。阅读下述流程,完成下列填空: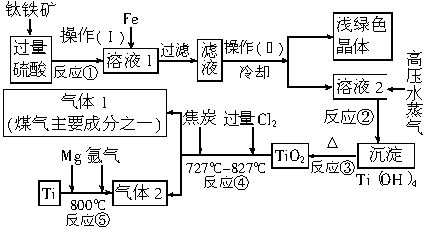
(1)操作(Ⅰ)中Fe的作用是____________,反应的离子方程式是_________________。
(2)操作(Ⅱ)的名称是______,得到的浅绿色晶体的化学式是__________________。
(3)写出反应④总的化学方程式(最终Ti的化合价不变):_____________________________。
(4)写出反应⑤的化学方程式:______________,
通入氩气的作用是____________________________。
(5)根据所提供的有关信息,你认为钛的用途之一是(指尖端科学技术)________________________。
(1)还原Fe3+;Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑
(2)(重)结晶、过滤;FeSO4?7H2O
(3)TiO2+2Cl2+2C
 TiCl4+2CO
TiCl4+2CO(或TiO2+2C
 Ti+2CO↑,Ti+2Cl2
Ti+2CO↑,Ti+2Cl2 TiCl4)
TiCl4)(4)TiCl4+2Mg
 Ti+2MgCl2;保护气作用
Ti+2MgCl2;保护气作用(5)制造潜艇或用做航天材料等

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
