题目内容
化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下表:编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
1 | Mg、Al | 稀盐酸 | 偏向Al |
2 | Al、Cu | 稀盐酸 | 偏向Cu |
3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
4 | Mg、Al | NaOH溶液 | 偏向Mg |
5 | Al、Zn | 浓硝酸 | 偏向Al |
试根据表中的实验现象完成下列问题:
(1)实验1、2中Al所作的电极是否相同?答:________________________。
(2)写出实验3中的电极反应式和电池总反应方程式。
铝为(____________)____________;石墨为(____________)_________;___________________。
(3)实验4中的铝作正极还是负极?答:____________,理由是________________________;写出铝电极的电极反应式:____________________________________。
(4)解释实验5中电流计指针偏向铝的原因:____________________________________。
(5)根据实验结果总结:在原电池中,铝作正极还是作负极受到哪些因素的影响?____________________________________________________________。
(1)不同
(2)负极 Al-3e-![]() Al3+ 正极 2H++2e-
Al3+ 正极 2H++2e-![]() H2↑ 2Al+6H+
H2↑ 2Al+6H+![]() 2Al3++3H2↑
2Al3++3H2↑
(3)负极 铝跟氢氧化钠溶液反应 Al+4OH--3e-![]()
![]() +2H2O
+2H2O
(4)铝在浓硝酸中钝化,锌为负极
(5)与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.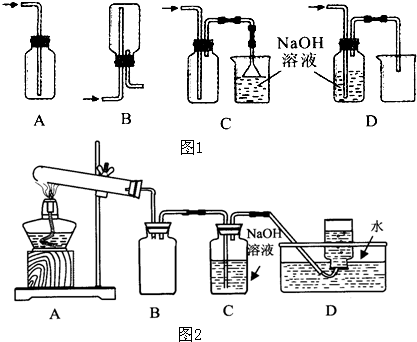
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验,如图1所示.
①写出该反应的离子方程式 ;
②下列收集Cl2的装置正确装置是 ;
③将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是 ;
④设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中, .
(2)某化学兴趣小组为了探究AgNO3的热稳定性,设计了如下实验.
用如图2所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束以后,试管中残留固体为黑色.
①装置B的作用是 .
②经小组讨论并验证该无色气体为O2,其验证方法是 .
【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】试管中残留的黑色固体可能是:ⅠAg;ⅡAg2O;ⅢAg和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
【实验评价】根据上述实验,③不能确定固体产物成分的实验是 (填实验编号).
【实验结论】根据上述实验结果,④该小组得出的AgNO3固体热分解的化学方程式为 .

(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验,如图1所示.
①写出该反应的离子方程式
②下列收集Cl2的装置正确装置是
③将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是
④设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,
(2)某化学兴趣小组为了探究AgNO3的热稳定性,设计了如下实验.
用如图2所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束以后,试管中残留固体为黑色.
①装置B的作用是
②经小组讨论并验证该无色气体为O2,其验证方法是
【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】试管中残留的黑色固体可能是:ⅠAg;ⅡAg2O;ⅢAg和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验结论】根据上述实验结果,④该小组得出的AgNO3固体热分解的化学方程式为
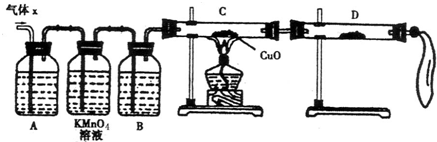
 某化学兴趣小组为了探究在常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.
某化学兴趣小组为了探究在常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想. (2011?宣城二模)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动:
(2011?宣城二模)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动: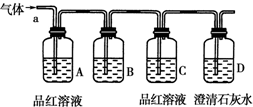 某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.
某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.