题目内容
【题目】下列各溶液中,微粒的物质的量浓度关系正确的是( )
A.![]()
![]() 的
的![]() 溶液中:
溶液中:![]()
B.![]() 的
的![]() 溶液中:
溶液中:![]()
C.![]() 的
的![]() 溶液与
溶液与![]() 的NaOH溶液等体积混合溶液显碱性,其混合溶液中:
的NaOH溶液等体积混合溶液显碱性,其混合溶液中:![]()
D.pH相等的![]() 、
、![]() 、
、![]() 三种溶液中,
三种溶液中,![]() 大小:
大小:![]()
【答案】D
【解析】
![]() 的
的![]() 溶液中,虽然铵根离子水解,但水解是微弱的,所以铵根离子浓度大于硫酸根离子浓度,由于铵根离子水解溶液显酸性,所以
溶液中,虽然铵根离子水解,但水解是微弱的,所以铵根离子浓度大于硫酸根离子浓度,由于铵根离子水解溶液显酸性,所以![]() ,故A错误;
,故A错误;
B.![]() 的
的![]() 溶液中存在质子守恒,水电离出的所有氢氧根离子浓度等于氢离子存在形式浓度总和,
溶液中存在质子守恒,水电离出的所有氢氧根离子浓度等于氢离子存在形式浓度总和,![]() ,故B错误;
,故B错误;
C.![]() 的
的![]() 溶液与
溶液与![]() 的NaOH溶液等体积混合得到等浓度的氯化铵、一水合氨和氯化钠溶液,溶液显碱性说明一水合氨电离程度大于铵根离子水解程度,
的NaOH溶液等体积混合得到等浓度的氯化铵、一水合氨和氯化钠溶液,溶液显碱性说明一水合氨电离程度大于铵根离子水解程度,![]() ,故C错误;
,故C错误;
D.相同pH的![]() 与
与![]() 溶液,都是强酸弱碱盐溶液,溶液显酸性的原因都是铵根离子的水解,而且硫酸根离子和氯离子对铵根离子的水解无影响,因此二者溶液中
溶液,都是强酸弱碱盐溶液,溶液显酸性的原因都是铵根离子的水解,而且硫酸根离子和氯离子对铵根离子的水解无影响,因此二者溶液中![]() 浓度相等,由于
浓度相等,由于![]() 电离时产生
电离时产生![]() 使溶液呈酸性,
使溶液呈酸性,![]() 水解产生的氢离子减少,因此
水解产生的氢离子减少,因此![]() 中
中![]() 的浓度小于
的浓度小于![]() ;则三种溶液中
;则三种溶液中![]() 由大到小的顺序为:
由大到小的顺序为:![]() ,故D正确;
,故D正确;
故选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
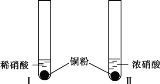
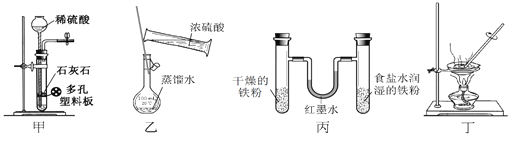
小学生10分钟应用题系列答案【题目】某学习小组探究稀HNO3、浓HNO3与铜的反应。
装置(尾气处理装置略) | 现象 |
| Ⅰ中开始无明显现象,渐有小气泡生成,越来越剧烈,液面上方出现浅红棕色气体,溶液呈蓝色。 |
Ⅱ中反应剧烈,迅速生成大量红棕色气体,溶液呈绿色。 |
(1)试管Ⅰ中Cu与稀HNO3反应的化学方程式是________。
(2)Ⅱ中反应的速率比Ⅰ中的快,原因是________。
(3)针对Ⅱ中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;
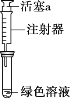
假设2:溶解了生成的NO2。
探究如下:取Ⅱ中绿色溶液,分为两等份。
①取一份于如图所示装置中,_______(填“操作”和“现象”),证实Ⅱ中溶解了NO2。
②向另一份溶液加入_____(填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1.HNO3浓度越稀,溶液中NO3-的数目越少,被还原时,每个NO3-从还原剂处获得较多电子的机会_____(填“增多”或“减少”),因此被还原为更低价态。
解释2.推测下列平衡导致了产物的不同,并通过如下实验证实了推测的合理性。
3NO2+H2O=2HNO3+NO
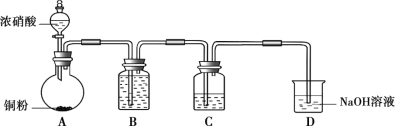
①B中盛放的试剂是________。
②C中盛放Cu(NO3)2和_________。
③该小组证实推测的合理性所依据的实验现象是________。