题目内容
【题目】NH3及其盐都是重要的化工原料。
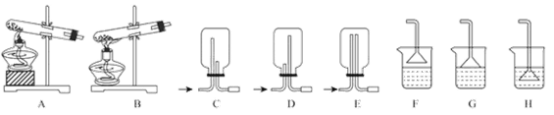
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为_____。
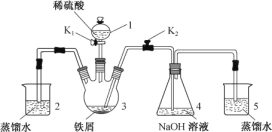
(2)按下图装置进行NH3性质实验。
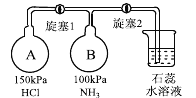
①先打开旋塞1,B瓶中的现象是_______,原因是__________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_________________。
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究______对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。_________________
物理量 | V(溶液)/mL | …… | |||
1 | 100 | ||||
2 | 100 |
③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应得平衡转化率
为_____(只列出算式,忽略水自身电离的影响)。
【答案】A、C、G 产生白烟 打开旋塞1,氯化氢与氨气混合反应生成了白色氯化铵固体小颗粒,形成白烟 烧杯中的石蕊溶液会倒流进入到B瓶中,形成红色溶液 温度(或浓度) 若探究温度对NH4Cl水解程度的影响时数据为:
物理量 | V(溶液)/mL | NH4Cl质量(g) | 温度(℃) | pH | …… |
1 | 100 | m | T1 | Y | |
2 | 100 | m | T2 | Z |
若探究浓度对NH4Cl水解程度的影响时数据为:
物理量 | V(溶液)/mL | NH4Cl质量(g) | 温度(℃) | pH | …… |
1 | 100 | m1 | T | Y | |
2 | 100 | m2 | T | Z |
(10-Y×5.35)/m
【解析】
(1)实验室用NH4Cl和Ca(OH)2制备NH3,依据反应条件和反应物状态确定发生装置;依据氨气易溶于水,密度小于空气密度选择收集装置;依据氨气极易溶于水特点选择尾气处理装置;
(2)①据AB容器压强及AB混合后压强相等,氨气和氯化氢反应生成白色固体氯化铵分析解答;
②氨气、氯化氢为气体,反应生成的氯化铵是固体,压强减小,氯化铵为强酸弱碱盐,溶液显酸性,据此解答;
(3)①根据影响NH4Cl水解的因素以及题干提供的限选试剂与仪器分析;
②氯化铵为强酸弱碱盐,水解溶液呈酸性,所配制溶液的体积,根据温度不同,盐类水解后PH不同,进行设计表格数据;
③读取的待测物理量的数值为Y,Y为pH值,pH=-lgc(H+)可求算出氢离子浓度,根据NH4++H2ONH3H2O+H+,求解NH4Cl水解反应的平衡转化率。
(1)NH4Cl和Ca(OH)2制备NH3是固体混合物加热制取气体的反应,有水生成,试管口应向下倾斜,发生装置选A,NH3密度比空气小,用向下排空气法收集,收集装置选C,氨气极易溶于水,要用防倒吸装置,但不能距离水太远,也不能插入液面以下,选G,故选A、C、G;
(2)①先打开旋塞1,B瓶中的现象是产生白色的烟;原因是先打开旋塞1,氯化氢与氨气挥发出来,氯化氢与氨气反应生成了氯化铵小颗粒,氯化铵小颗粒形成白烟;
②再打开旋塞2,B瓶中的现象是烧杯中的石蕊溶液会倒流进入到B瓶中,是因为气体参与反应后使得烧瓶内的压强变小,打开旋塞2后,大气压就会把烧杯中的溶液压到烧瓶中来,同时由于A中的HCl不可能全部进入B中,A中HCl过量,就算不能完全进入B瓶,B中的氨气也应能完全反应,形成氯化铵,石蕊溶液进入B中,B中的NH4Cl溶于石蕊溶液,溶液显酸性,所以石蕊试液显红色;
(3)①主要采用控制变量的方法,根据给出的仪器,有可控制温度水浴槽,那么可以完成温度对NH4Cl水解程度的影响,天平可以称出不同质量NH4Cl,那么可以配制出不同浓度的溶液,就可以探究浓度对NH4Cl水解程度的影响,故答案为温度或浓度。
①如果探究温度的影响那么控制浓度相同,改变温度,如果探究浓度相同,那么就要控制温度相同,不管哪一种探究都需要配制一定浓度的NH4Cl溶液,那么需要称量NH4Cl的质量,但不管探究的是哪种因素的影响,都需要使用pH计通过测量水解后溶液的pH来判断其水解程度,所以在表格中都应有一项为pH值。
若探究温度对NH4Cl水解程度的影响时数据为:
物理量 | V(溶液)/mL | NH4Cl质量(g) | 温度(℃) | pH | …… |
1 | 100 | m | T1 | Y | |
2 | 100 | m | T2 | Z |
若探究浓度对NH4Cl水解程度的影响时数据为:
物理量 | V(溶液)/mL | NH4Cl质量(g) | 温度(℃) | pH | …… |
1 | 100 | m1 | T | Y | |
2 | 100 | m2 | T | Z |
如果pH 为Y,那么c(H+)=10-Ymol/L,物质的量为10-Ymol/L×0.1L=10-Y-1mol,那么水解的NH4Cl的物质的量也为10-Y-1mol,质量为10-Y-1mol×53.5g/mol=10-Y×5.35g,则NH4Cl水解反应得平衡转化率为:( 10-Y×5.35)/m。

 阅读快车系列答案
阅读快车系列答案【题目】用如图装置制取并收集气体,对应的装置和试剂均正确的是( )
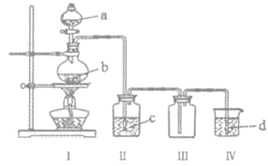
Ⅲ收集气体 | Ⅰ中试剂a,b | Ⅱ中试剂c | Ⅳ中试剂d | |
A | SO2 | 稀硫酸与铜片 | 浓硫酸 | NaOH溶液 |
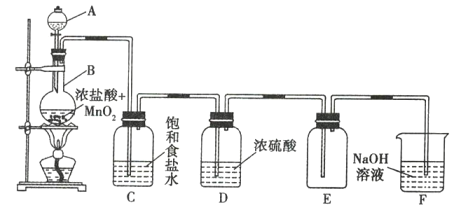
B | Cl2 | 浓盐酸与二氧化锰 | 饱和氯化钠溶液 | NaOH 溶液 |
C | HBr | 浓硫酸与溴化钠 | 浓硫酸 | 水 |
D | CO | 甲酸与浓硫酸 | 浓硫酸 | 酸性KMnO4溶液 |
A. AB. BC. CD. D