题目内容
【题目】下列物质溶于水因水解而呈碱性的是
A. Na2O B. Na2CO3 C. NH4Cl D. NH3 ·H2O
【答案】B
【解析】
A.Na2O溶于水,与水发生反应产生NaOH,是发生化合反应产生碱,电离使溶液显碱性,A不符合题意;
B.Na2CO3是强碱弱酸盐,在溶液中CO32-与水电离产生的H+结合形成HCO3-,使溶液中c(OH-)>c(H+),因此溶液显碱性,是由于盐水解所致,B符合题意;
C.NH4Cl是强酸弱碱盐,在溶液中NH4+与水电离产生的OH-结合形成NH3H2O,使溶液中c(H+)>c(OH-),因此溶液显酸性,是由于盐水解所致,C不符合题意;
D. NH3 ·H2O是一元弱碱,在水溶液中会发生电离:NH3 ·H2O![]() NH4++OH-,与盐的水解无关,D不符合题意;
NH4++OH-,与盐的水解无关,D不符合题意;
故合理选项是B。

 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
实验室用干燥、纯净的二氧化硫和氯气合成硫酰氯,装置如图所示(夹持仪器已省略),请回答有关问题:
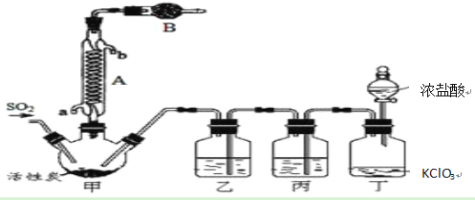
(1)仪器A冷却水的进水口为________(填“a”或“b”)。
(2)仪器B中盛放的药品是________,其目的是________________________。
(3)实验时,装置丁中发生反应的离子方程式为______________________________,当生成6.72L的氯气(标况下),转移电子的物质的量为________。
(4)装置丙中盛放的试剂是________,若缺少装置乙,对实验造成的影响是_______________。
(5)少量硫酰氯也可用液态氯磺酸(ClSO3H)低温催化分解获得,该反应的化学方程式为:2ClSO3H=H2SO4 +SO2Cl2,从分解产物中分离出硫酰氯的操作是______________。