题目内容
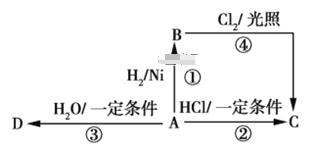
【题目】三个装有CH4和Cl2 混合气体的集气瓶,用玻璃片盖好瓶口后,分别作如下处理,各有怎样的现象发生?
(1)①置于黑暗中: _____________________;
②将点燃的镁条靠近集气瓶外壁: ________________________;
③放在有光线的房子里: __________________________________。
(2)CH4和Cl2发生的一系列反应都是___________(填反应类型)反应,请写出CH4和Cl2反应生成一氯甲烷的化学方程式: ________________________________。
(3)若要使0.5 mol CH4完全和Cl2发生取代反应,并生成相同物质的量的四种取代产物,则生成HCl的物质的量为_________。
A.2.5mol B.2mol C.1.25mol D.0.5mol
【答案】①无明显现象 ②爆炸 ③黄绿色逐渐变浅,有油状液滴生成 取代 CH4+Cl2![]() CH3Cl+HCl C
CH3Cl+HCl C
【解析】
(1)①根据甲烷和氯气反应的条件解答;
②点燃的镁条放热;
③根据甲烷与氯气反应的产物的性质解答;
(2)甲烷和氯气发生反应,甲烷分子中的氢原子被氯原子取代.
(3)先根据碳原子守恒计算四种有机物的物质的量,氯气发生的取代反应是1个氯原子替换出1个氢原子,另一个氯原子则与氢原子结合生成氯化氢,从氢原子、氯原子守恒的角度分析;
(1)①甲烷与氯气反应须在光照的条件下反应,所以,在黑暗的条件下,无明显现象;
②镁和氧气在点燃的条件下发生反应,放出的热量,同时产生耀眼的强光,使CH4和Cl2 混合气体能在光照时发生取代反应,该反应放出热量,是气体体积急剧膨胀发生爆炸现象;
③甲烷与氯气反应,可生成有机物有CH3Cl、CH2Cl2、CHCl3、CCl4等,其中二氯甲烷、三氯甲烷与四氯甲烷为油状液体,因此放在有光线的房子里,黄绿色的氯气被逐步反应消耗,会看到气体的颜色变浅,有油状液滴生成;
(2)甲烷与氯气在光照下发生取代反应,甲烷分子中的氢原子被氯气分子中的氯原子取代,生成一氯甲烷和氯化氢,故答案为:取代;CH4+Cl2![]() CH3Cl+HCl;
CH3Cl+HCl;
(3)0.5molCH4生成等物质的量的4种取代产物,即0.125mol CH3Cl、0.125molCH2Cl2、0.125 molCHCl3、0.125 molCCl4,生成HCl的物质的量为n(HCl)=0.125 mol×l+0.125mol×2+ 0.125mol×3+0.125mol×4=1.25mol,故合理选项是C。

 活力课时同步练习册系列答案
活力课时同步练习册系列答案【题目】绿水青山就是金山银山,研究NO2, NO,CO,SO2 等大气污染物和温室效应的治理对建设美丽中国具有重要意义。
(1)已知:NO2(g)+CO(g) ![]() CO2(g)+NO(g) 该反应的平衡常数为K1(下同),每1mol下列物质分解为气态基态原子吸收的能量分别为
CO2(g)+NO(g) 该反应的平衡常数为K1(下同),每1mol下列物质分解为气态基态原子吸收的能量分别为
NO2, | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②N2(g)+O2(g)═2NO(g)△H=+179.5kJmol1 k2
③2NO(g)+O2(g)═2NO2(g)△H=112.3kJmol1 k3
写出NO与CO反应生成无污染气体的热化学方程式为____________.该热化学方程式的平衡常数K为______________(用K1。K2。K3表示)。
(2)用焦炭还原NO的反应为:2NO(g)+C(s)![]() N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:

①该反应为________(填“放热”或“吸热”)反应。
②乙容器在60min时达到平衡状态,则0~60min内用NO的浓度变化表示的平均反应速率v(NO)=____________。
(3)在体积可变的恒压密闭容器中充入1molCO2与足量的碳,让其发生反应:C(s)+CO2(g) ![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:

T℃时,若容器中充入惰性气体,v正 ______ v逆(填<,>,=),平衡______移动(填正向,逆向或不。下同),若充入等体积的CO2和CO,平衡_________移动。
650℃时,反应达平衡后CO2的转化率为________。