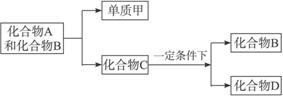
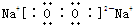题目内容
常温下 A 和 B 两种气体组成混合气体(A 的相对分子质量大于 B 的相对分子质量),经分析混合气体中只含有碳和氢两种元素,而且不论 A 和 B 以何种比例混合,碳和氢的质量比总小于 3∶1。由此可确定 A 为_____________,B 为____________,其理由是__________________。
若上述混合气体中碳和氢的质量比为9∶4,则在混合气体中 A 和 B 的物质的量之比为________;A 在混合气体中的体积分数为_____%。
A:CH4 B:H2 CH4中碳氢质量比为 3∶1,是气态烃中碳、氢质量比最小的,若使碳氢质量比比 3∶1 还要小,只有在 CH4中混入 H2 才能满足要求 3∶2 60%
解析:
解答此题,首先从碳、氢元素形成的化合物中寻找碳氢元素质量比为 3∶1 者。CH4中,m(C)∶m(H)=12∶4=3∶1。题设条件下,m(C)∶m(H)<3∶1,这只能在 CH4中混入 H2 (CH4中若混入其他碳氢化合物,如 C2H2,只能使m(C)∶m(H)>3∶1)。由于Mr(A)>Mr(B),所以 A 为 CH4,B 为 H2。
设混合气体中 A、B 物质的量分别为 x 和 y。则“xCH4+yH2”中,12x∶(4x+2y)=9∶4,解得,x∶y=3∶2,![]() (A)=(3÷5)×100%=60%。
(A)=(3÷5)×100%=60%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目