题目内容
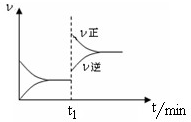 如图为某化学反应的速率与时间的关系示意图.下列有关t1时刻改变条件的说法正确的是( )
如图为某化学反应的速率与时间的关系示意图.下列有关t1时刻改变条件的说法正确的是( )分析:由图可知t1时刻,正逆反应速率均增大,且正反应速率大于逆反应速率,则改变的条件为升高温度或增大压强,且反应向正反应方向移动,以此来解答.
解答:解:A.该反应为放热反应,升高温度,平衡逆向移动,逆反应速率大于正反应速率,与图象不符,故A错误;
B.增大氧气的浓度,瞬间逆反应速率不变,与图象不符,故B错误;
C.该反应为气体体积不变的反应,增大压强,正逆反应速率同等程度的增大,与图象不符,故C错误;
D.该放热为吸热反应,升高温度,平衡正向移动,正逆反应速率均增大,且正反应速率大于逆反应速率,与图象相符,故D正确;
故选D.
B.增大氧气的浓度,瞬间逆反应速率不变,与图象不符,故B错误;
C.该反应为气体体积不变的反应,增大压强,正逆反应速率同等程度的增大,与图象不符,故C错误;
D.该放热为吸热反应,升高温度,平衡正向移动,正逆反应速率均增大,且正反应速率大于逆反应速率,与图象相符,故D正确;
故选D.
点评:本题考查影响反应速率的因素,注意图象中的速率变化及外界因素对反应速率的影响即可解答,题目难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
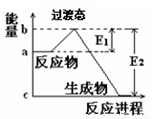
(8分)(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是 (填“吸热”或“放热”)反应,NO2和CO的总能量 (填“>”、“<”或“=”)CO2和NO的总能量。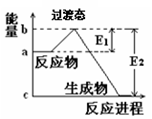
(2)在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:
NO2+CO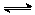 CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
①该段时间内,用CO2表示的平均反应速为 。
②假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量为 。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
| A.容器内气体的质量保持变 | B.NO2的物质的量浓度不再改变 |
| C.容器内气体的平均相对分子质量不变 | D.NO2的消耗速率与CO2的消耗速率相等 |
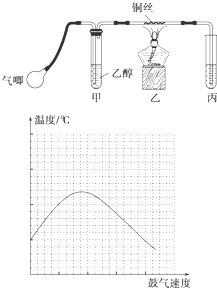 某研究性学习小组的同学利用如图所示装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.
某研究性学习小组的同学利用如图所示装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.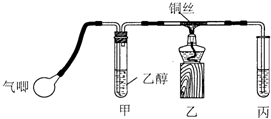
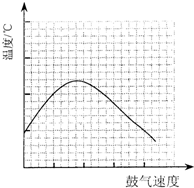

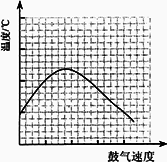
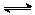 CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则: