题目内容
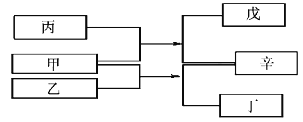
【题目】A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体。常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示。下列说法正确的是
A. 元素B、C、D的原子半径由大到小的顺序为 r(D)>r(C)>r(B)
B. 1L0.lmol/L戊溶液中阴离子的总物质的量小于0.1mol
C. 1mol甲与足量的乙完全反应共转移了约6.02×1023个电子
D. 元素的非金属性B > C > A
【答案】C
【解析】常温下,0.1mol/L 丁溶液的pH为13,丁是一元强碱,为NaOH,发生甲+乙=丁+辛,甲、乙中含H、O、Na,辛是由C元素形成的单质为O2,故甲为Na2O2,乙是水,再由甲+丙=戊+辛,可知丙为CO2,戊是Na2CO3,四种元素分别是H、C、O、Na。
A、同周期,从左到右,原子半径随着原子序数的递增,半径逐渐减小,同主族,从上到下,原子半径随着原子序数的递增,半径逐渐增大,原子半径大小顺序为Na、C、O,故A错误;B、Na2CO3中CO32―要部分水解,CO32-+H2O![]() HCO3-+OH-,HCO3-+H2O
HCO3-+OH-,HCO3-+H2O![]() H2CO3+OH-,由电荷守恒可知,1molCO32―可水解生成2molOH― , 1L0.lmol/L戊溶液中阴离子的总物质的量大于0.1mol,故B错误;C、由2Na2O2+2H2O=4NaOH+O2,每1molNa2O2反应转移1mol电子,故C正确;D、元素的金属性与非金属性(1)同一周期的元素从左到右金属性递减,非金属性递增;(2)同一主族元素从上到下金属性递增,非金属性递减,元素的非金属性应是O > C ,故D错误。故选C。
H2CO3+OH-,由电荷守恒可知,1molCO32―可水解生成2molOH― , 1L0.lmol/L戊溶液中阴离子的总物质的量大于0.1mol,故B错误;C、由2Na2O2+2H2O=4NaOH+O2,每1molNa2O2反应转移1mol电子,故C正确;D、元素的金属性与非金属性(1)同一周期的元素从左到右金属性递减,非金属性递增;(2)同一主族元素从上到下金属性递增,非金属性递减,元素的非金属性应是O > C ,故D错误。故选C。

 初中暑期衔接系列答案
初中暑期衔接系列答案

