��Ŀ����
(14��)�� ֪�������·�Ӧ��
֪�������·�Ӧ��

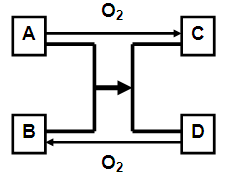
����A��CΪ�����������ʣ�B��DΪ��������B���д��ԣ�EΪ��ɫ���嵥�ʡ�
�ݴ˻ش�
��1��D������ǿ���ǿ�д��D������������Һ��Ӧ�����ӷ���ʽ
��
��2������E�� ���ѧʽ�����ڷ�Ӧ���У�1mol B������Ӧʱת�Ƶ��ӵ����ʵ����� ��
��3��������A��C�õ������ӣ���ϡ���ṹ��ԭ��أ����ԭ��صĸ����� ����Ԫ�ط��ţ��������ĵ缫��Ӧʽ�� ��
��4��B�����ϡ����������������һ����ɫ���壬д���˷�Ӧ�����ӷ���ʽ
��
����B���������п��γ���ҺF��F�д��ڵ����ֽ����������� �������ӷ��ţ���
������ �����ּ���F�еĵͼ۽��������ӵ�ʵ�鷽��������ʵ�鲽�輰Ԥ��ʵ������
�����ּ���F�еĵͼ۽��������ӵ�ʵ�鷽��������ʵ�鲽�輰Ԥ��ʵ������
�ֱ�ȡ����F��Һ����֧�ྻ���Թ��У�
�����һ֧�Թ��еμ�KSCN ��Һ����Һ����ɫ���ٵμ���ˮ����Һ���ɫ��
��Һ����Һ����ɫ���ٵμ���ˮ����Һ���ɫ��
����ڶ�֧�Թ�����Һ�ĵײ��õι�ע�� NaOH��Һ�����ɰ�ɫ������Ȼ��Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��
NaOH��Һ�����ɰ�ɫ������Ȼ��Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��
�������֧�Թ��еμ�����KMnO4��Һ����KMnO4��Һ��ɫ��ȥ��
�������ַ����к������� ����١��ڻ�ۣ���
������ҺF�м�������ͭ�ۣ���ͭ�����ܽ⣬��д���˹����з�����Ӧ�����ӷ���ʽ
 ��
��
 ֪�������·�Ӧ��
֪�������·�Ӧ��
����A��CΪ�����������ʣ�B��DΪ��������B���д��ԣ�EΪ��ɫ���嵥�ʡ�
�ݴ˻ش�
��1��D������ǿ���ǿ�д��D������������Һ��Ӧ�����ӷ���ʽ
��
��2������E�� ���ѧʽ�����ڷ�Ӧ���У�1mol B������Ӧʱת�Ƶ��ӵ����ʵ����� ��
��3��������A��C�õ������ӣ���ϡ���ṹ��ԭ��أ����ԭ��صĸ����� ����Ԫ�ط��ţ��������ĵ缫��Ӧʽ�� ��
��4��B�����ϡ����������������һ����ɫ���壬д���˷�Ӧ�����ӷ���ʽ
��
����B���������п��γ���ҺF��F�д��ڵ����ֽ����������� �������ӷ��ţ���
������
 �����ּ���F�еĵͼ۽��������ӵ�ʵ�鷽��������ʵ�鲽�輰Ԥ��ʵ������
�����ּ���F�еĵͼ۽��������ӵ�ʵ�鷽��������ʵ�鲽�輰Ԥ��ʵ�������ֱ�ȡ����F��Һ����֧�ྻ���Թ��У�
�����һ֧�Թ��еμ�KSCN
 ��Һ����Һ����ɫ���ٵμ���ˮ����Һ���ɫ��
��Һ����Һ����ɫ���ٵμ���ˮ����Һ���ɫ������ڶ�֧�Թ�����Һ�ĵײ��õι�ע��
 NaOH��Һ�����ɰ�ɫ������Ȼ��Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��
NaOH��Һ�����ɰ�ɫ������Ȼ��Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ���������֧�Թ��еμ�����KMnO4��Һ����KMnO4��Һ��ɫ��ȥ��
�������ַ����к������� ����١��ڻ�ۣ���
������ҺF�м�������ͭ�ۣ���ͭ�����ܽ⣬��д���˹����з�����Ӧ�����ӷ���ʽ

 ��
����14�֣���1��Al2O3 + 2OH�� = 2AlO2�� + H2O��2�֣���2��O2��1�֣� 8mol��2�֣�
(3)Al��1�֣� 2H+ + 2e�� = H2����2�֣� (4) 3Fe3O4 + 28H+ + NO3�� = 9Fe3+ + NO�� + 14H2O��2�֣�
Fe2+��Fe3+��1�֣��ۣ�1�֣�2Fe3+ + Cu = 2Fe2+ + Cu2+��2�֣�
(3)Al��1�֣� 2H+ + 2e�� = H2����2�֣� (4) 3Fe3O4 + 28H+ + NO3�� = 9Fe3+ + NO�� + 14H2O��2�֣�
Fe2+��Fe3+��1�֣��ۣ�1�֣�2Fe3+ + Cu = 2Fe2+ + Cu2+��2�֣�
��

��ϰ��ϵ�д�
�����Ŀ