题目内容
(1)写出Na2O2和SO2之间反应的化学方程式________.
(2)碱金属与O2反应生成氧化物比较复杂,有普通氧化物如Na2O,过氧化物如Na2O2等,甚至有超氧化物,臭氧化物,因此要制备碱金属普通氧化物,一般用碱金属还原对应过氧化物,硝酸盐等.用化学方程式表示以下反应.
①钠与过氧化钠反应________;
②钾与硝酸钾反应时还生成一种单质,化学方程式为________;
此反应为什么不会生成K2O2?说明理由________.

 名校课堂系列答案
名校课堂系列答案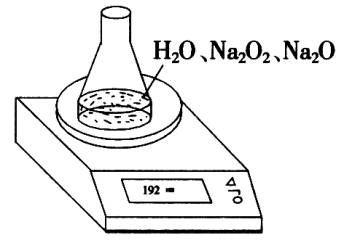
|
|
读数次数 |
质量(g) |
|
|
第1次 |
192.214 |
|
|
第2次 |
192.164 |
|
锥形瓶+水+试样 |
第3次 |
192.028 |
|
|
第4次 |
192.010 |
|
|
第5次 |
192.010 |
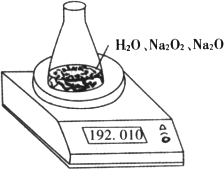
(1)写出Na2O2和H2O反应的化学方程式__________.
(2)计算过氧化钠质量分数时,必需的数据是________,不必作第6次读数的原因是________.
(3)测定上述样品(1.560g)中Na2O2质量分数的另一种方案,其操作流程如下:
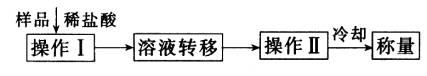
①操作Ⅱ的名称是________.
②需直接测定的物理量是________.
③测定过程中需要的仪器有电子天平、蒸发皿、酒精灯,还需要________、________(固定、夹持仪器除外).
④在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果________(填“偏大”、 “偏小”或“不变”).
| |||||||||||||||

| 读数次数 | 质量(g) |
锥形瓶+水+试样 | 第一次 | 192.214 |
第二次 | 192.164 | |
第三次 | 192.028 | |
第四次 | 192.010 | |
第五次 | 192.010 |
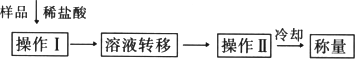
(1)写出Na2O2和H2O反应的化学方程式 。
(2)计算过氧化钠的质量分数时,必需的数据是 ,不必作第六次读数的原因是 。
(3)测定上述样品(
![]()
①操作Ⅱ的名称是 。
②需直接测定的物理量是 。
③测定过程中需要的仪器有电子天平、蒸发皿、酒精灯,还需要 、 (固定、夹持仪器除外)。
④在转移溶液时,如溶液转移不完全,则Na2O2的质量分数的测定结果 (填“偏大”“偏小”或“不变”)。