题目内容
11.分别将9.2g Na投入100g下列溶液中:①0.365%盐酸;②3.65%盐酸;③36.5%盐酸,放出氢气的量( )| A. | ①最多 | B. | ③最多 | C. | 一样多 | D. | 无法判断 |
分析 n(Na)=$\frac{9.2g}{23g/mol}$=0.4mol,可与水发生:2Na+2H2O=2NaOH+H2↑,或与酸发生2Na+2HCl=2NaCl+H2↑,结合方程式解答该题.
解答 解:n(Na)=$\frac{9.2g}{23g/mol}$=0.4mol,可与水发生:2Na+2H2O=2NaOH+H2↑,或与酸发生2Na+2HCl=2NaCl+H2↑,
①②溶液中m(H2O)≥90g,n(H2O)≥5mol,
③中$\frac{100g×36.5%}{36.5g/mol}$=1mol,酸足量,
Na均完全反应,则生成氢气的质量相等.
故选C.
点评 本题考查化学方程式的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,难度中等,注意水的量为解答该题的关键.

练习册系列答案
相关题目
20.在限定条件下,下列溶液中各组离子一定能大量共存的是( )
| A. | 使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- | |
| B. | 与Al能产生氢气的溶液:K+、SO42-、HCO3-、NH4+ | |
| C. | 碳酸氢钠溶液:K+、Na+、Cl-、SO42- | |
| D. | 常温下pH<7的溶液:K+、SiO32-、Na+、AlO2- |
9.某温度下,H2(g)+CO2(g)?H2O(g)+CO(g)的平衡常数K=$\frac{9}{4}$.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示.
下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
| A. | 平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L | |
| B. | 反应开始时,丙中的反应速率最快,甲中的反应速率最慢 | |
| C. | 平衡时,乙中CO2的转化率大于60% | |
| D. | 平衡时,甲中和丙中H2的转化率均是60% |
 .
. .
.
 ;C:
;C: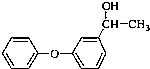 .
.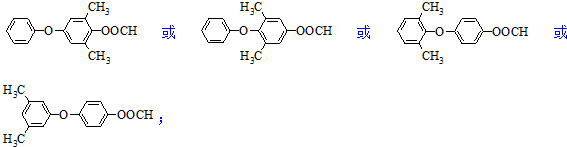 .
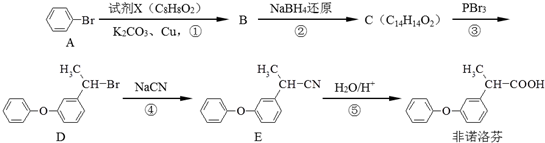
.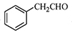 为原料制备
为原料制备 的合成路线流程图如下:
的合成路线流程图如下: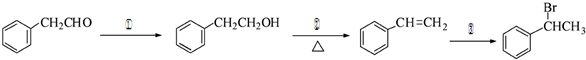
 800℃时,某密闭容器中存在如下反应:2NO2(g)?2NO(g)+O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的产率随时间的变化如图曲线I所示.
800℃时,某密闭容器中存在如下反应:2NO2(g)?2NO(g)+O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的产率随时间的变化如图曲线I所示.