题目内容
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
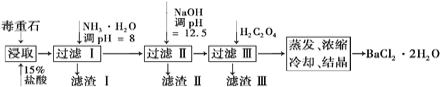
(1)毒重石用盐酸浸取前需充分研磨,目的是________。实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中的________。
a.烧杯 b.500mL容量瓶 c.玻璃棒 d.滴定管
(2)已知不同杂质离子开始沉淀和沉淀完全的pH如下:

加入NH3·H2O调节pH=8可除去_______ (填离子符号),此时,溶液中该离子的浓度为_______mol·L-1。加入NaOH调pH=12.5,溶液内剩余的阳离子中_______完全沉淀,_____________ (填离子符号)部分沉淀。加入H2C2O4时应避免过量,原因是___________。(已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9, Ksp[Fe(OH)3] =2.6×10-39)
【答案】增大接触面积从而使反应速率加快 ac Fe3+ 2.6×10-21 Mg2+ Ca2+ H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少
【解析】
制备BaCl22H2O的流程:毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),加盐酸溶解,碳酸钡和盐酸反应:BaCO3+2H+=Ba2++CO2↑+H2O,加入氨水,调pH为8,Fe3+完全沉淀时的pH为3.2,只有Fe3+完全沉淀,滤渣1为Fe(OH)3,溶液中主要含Ca2+、Mg2+、Ba2+,加入氢氧化钠调节pH=12.5,Ca2+完全沉淀时的pH为13.9,Mg2+完全沉淀时的pH为11.1,Mg2+完全沉淀,Ca2+部分沉淀,滤渣Ⅱ中含Mg(OH)2、Ca(OH)2;溶液中主要含Ca2+、Ba2+,加入H2C2O4,得到CaC2O4↓,除去Ca2+,蒸发浓缩冷却结晶得到BaCl22H2O;
(1)研磨将块状固体变成粉末状,可以增大反应物的接触面积,增大反应速率;溶液中质量分数=![]() ×100%,实验室用37%的盐酸配置15%的盐酸,需量取浓盐酸的体积和水的体积,且需使用烧杯作为容器稀释,玻璃棒搅拌;
×100%,实验室用37%的盐酸配置15%的盐酸,需量取浓盐酸的体积和水的体积,且需使用烧杯作为容器稀释,玻璃棒搅拌;
(2)根据流程图和表中数据分析加入NH3H2O调节pH=8可除去Fe3+,加入NaOH调pH=12.5,可完全除去Mg2+,除去部分Ca2+;加入过量H2C2O4,易发生Ba2++H2C2O4═BaC2O4↓+2H+,产品的产量减少。
(1)化学反应的速率与反应物的接触面积有关,毒重石用盐酸浸取前需充分研磨,可以增大反应物的接触面积,增大反应速率,溶液中质量分数=![]() ×100%,实验室用37%的盐酸配置15%的盐酸,需计算出浓盐酸的体积和水的体积,需用量筒量取,浓盐酸稀释为稀盐酸,需用烧杯作为容器稀释选择a,玻璃棒搅拌加速溶解选择c,故答案为ac;
×100%,实验室用37%的盐酸配置15%的盐酸,需计算出浓盐酸的体积和水的体积,需用量筒量取,浓盐酸稀释为稀盐酸,需用烧杯作为容器稀释选择a,玻璃棒搅拌加速溶解选择c,故答案为ac;
(2)根据流程图和表中数据可知:Fe3+完全沉淀时的pH为3.2,加入氨水,调pH为8,Fe3++3NH3H2O=Fe(OH)3↓+3NH4+,Fe3+完全沉淀,滤渣1为Fe(OH)3,由Ksp[Fe(OH)3] =c(Fe3+)×c3(OH-)=2.6×10-39,pH为8,c(OH-)=1×10-6mol/L,则c(Fe3+)= mol/L=2.6×10-21 mol/L;加入氢氧化钠调节pH=12.5,Ca2+完全沉淀时的pH为13.9,Mg2+完全沉淀时的pH为11.1,Mg2+完全沉淀,Ca2+部分沉淀,滤渣Ⅱ中含Mg(OH)2、Ca(OH)2,溶液中主要含Ca2+、Ba2+,Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9,易形成CaC2O4沉淀,加入H2C2O4时应避免过量,防止CaC2O4沉淀完全后,过量的H2C2O4会导致生成BaC2O4沉淀,产品的产量减少。
mol/L=2.6×10-21 mol/L;加入氢氧化钠调节pH=12.5,Ca2+完全沉淀时的pH为13.9,Mg2+完全沉淀时的pH为11.1,Mg2+完全沉淀,Ca2+部分沉淀,滤渣Ⅱ中含Mg(OH)2、Ca(OH)2,溶液中主要含Ca2+、Ba2+,Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9,易形成CaC2O4沉淀,加入H2C2O4时应避免过量,防止CaC2O4沉淀完全后,过量的H2C2O4会导致生成BaC2O4沉淀,产品的产量减少。

 阅读快车系列答案
阅读快车系列答案