题目内容
【题目】下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液稀释至10倍后pH=4
C.0.2 mol/L的盐酸与0.1 mol/L的盐酸等体积水混合后pH=1.5
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH<7
【答案】D
【解析】解:A、加热会促进水的电离,故95℃时,纯水的pH<7,但纯水永远显中性,故A错误;
B、醋酸是弱电解质,加水稀释电离被促进,故加水稀释10倍后溶液的pH<4,故B错误;
C、酸和酸混合后溶液显酸性,混合后溶液中的c(H+)= ![]() =
= ![]() =0.15mol/L,则pH=﹣lg0.15≠1.5,故C错误;
=0.15mol/L,则pH=﹣lg0.15≠1.5,故C错误;
D、醋酸是弱酸,不完全电离,故当pH=3的醋酸和pH=11的氢氧化钠溶液混合后,醋酸过量,溶液显酸性,即pH<7,故D正确.
故选D.
【考点精析】解答此题的关键在于理解弱电解质在水溶液中的电离平衡的相关知识,掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.

 阅读快车系列答案
阅读快车系列答案【题目】某学习小组用如下装置(支撑仪器略去)探究乙醇的催化氧化反应和乙醛的性质. 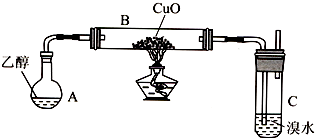
(1)实验开始时,对A进行水浴加热,其目的是 .
(2)B中反应方程式为 .
(3)若装置C中开始发生倒吸,则采取的应急措施是(填编号).
A.移去图中的酒精灯
B.将C中橡皮塞上的短导气管拔出
C.将B尾端的乳胶管取下
D.将A与B之间的乳胶管取下
(4)探究:充分反应后,观察到溴水完全褪色.学习小组通过测定反应前溴水中n(Br2)与反应后溶液中n(Br﹣)来确定乙醛使溴水褪色的原因. ①假设.请写出假设1的反应类型.
假设1:CH3CHO+Br2→CH2BrCHO+HBr;反应
假设2:CH3CHO+Br2→CH3CHBrOBr; 加成反应
假设3:CH3CHO+Br2+H2O→CH3COOH+2HBr. 氧化反应
②结论:若实验测得n(Br2)=0.005mol,n(Br﹣)=0.01mol,则证明假设正确.
(5)欲检验乙醇中混有的少量乙醛,甲乙丙三同学设计实验如表:
试剂、用品 | 预期现象 | |
甲 | 酸性高锰酸钾溶液 | 溶液紫红色褪去 |
乙 | 溴水 | 溴水褪色 |
丙 | 铜丝 酒精灯 | 铜丝由黑色变成光亮的红色 |
则上述方案中你认为能正确完成乙醛的检验的是(填甲、乙、丙)
【题目】在25℃时,密闭容器中X,Y,Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数