��Ŀ����
����Ŀ������ͼ��ʾ��ʵ��װ�ý��е绯ѧʵ�飬�����ж���ȷ����( )
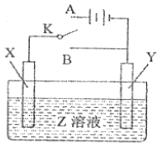
A. ��XΪ��Ƭ��YΪþƬ��ZΪNaOH��������K����B����YΪԭ��صĸ���
B. ��XΪͭƬ��YΪ��Ƭ��ZΪCuSO4��������K����A����ʵ������Ƭ�϶�ͭ
C. ��XΪ��Ƭ��YΪпƬ��ZΪNaCl��������K����A��B�����ɼ������ĸ�ʴ
D. ��X��Y��Ϊ̼����ZΪNaOH��������K����A����Y�������ķ�ӦΪ2H++2e-=H2��
���𰸡�B
��������A. ��XΪ��Ƭ��YΪþƬ��ZΪNaOH��������K����B�����γ�ԭ��أ������ķ�ӦΪ��������������Һ��Ӧ������Ϊԭ��صĸ�������A����B. ��XΪͭƬ��YΪ��Ƭ��ZΪCuSO4��������K����A�����̵��أ�ͭΪ��������Ϊ��������ʵ������Ƭ�϶�ͭ����B��ȷ��C. ��XΪ��Ƭ��YΪпƬ��ZΪNaCl��������K����A�����ɵ��أ���Ϊ��������ʴ���ʼӿ죬��C����D. ��X��Y��Ϊ̼����ZΪNaOH��������K����A�����ɵ��أ��������ϵ��ˮ��Y��Ϊ��������Һ��ˮ�õ������������������������ӣ�2H2O+2e- = H2��+ 2OH�D����D����ѡB��

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�����Ŀ��ijС��ͬѧ���о�SO2�����ʡ�
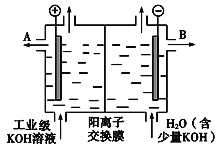
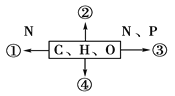
(1)����صĺ������ʷ�Ϊ���±���ʾ3�飬��2��������X�Ļ�ѧʽ�� ��
��1�� | ��2�� | ��3�� |
S(����) | SO2��X��Na2SO3��NaHSO3 | SO3��H2SO4��Na2SO4��NaHSO4 |
(2)������ͼ��ʾ��װ���о�SO2�����ʣ�
(�۵㣺SO2 ��76.1����SO3 16.8�����е㣺SO2 ��10����SO3 45��)

��װ����ģ�ҵ������SO2�������ķ�Ӧ���仯ѧ����ʽ�� ��
����ͬѧ������������������˳������װ�ã�װ������������ ��װ��������Һ����ɫ������Mn2+��ͬʱpH���ͣ���÷�Ӧ�����ӷ���ʽ�� ��
����ͬѧ��������������˳������װ�ã���װ��������40 mL 2.5mol/L NaOH��Һ����Ӧ������4.8 g����װ�����з�����Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�(1)H2SO3 (2)��2SO2��O2![]() 2SO3
2SO3
��ʹSO3����ɹ�����SO2���� 5SO2��2H2O��2MnO4����5SO42����2Mn2����4H��
��3SO2��4NaOH��Na2SO3��2NaHSO3��H2O
��������
��1���۲�������֪���ڶ�����X����Ӧ���������+4�۵ĺ����ᣬ��������
��2����SO2��V2O5�Ĵ������¿ɱ�����ΪSO3
�����������ݿ�֪SO3�ڱ�ˮ�гʹ�̬������IIװ����ͨ������������������
SO2�ɽ�����KMnO4�е���Ԫ�ػ�ԭ�����������ɣ���ҺpH���ͣ����ʷ�Ӧ����ʽΪ��5SO2+ 2H2O + 2MnO4��="=" 5SO42��+ 2Mn2++ 4H+
��SO2��NaOH��Һ��Ӧ�����ߵ����ʵ������йأ�
SO2+ 2NaOH = Na2SO3+ H2O SO2+ NaOH =NaHSO3
�����ߵ����ʵ�����Ϊ4:7��ֱ�����ܷ���ʽ����Ԫ���غ�����ƽ����
�����͡�ʵ����
��������
29
����Ŀ����ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�����ѹ������Ͳ�ڣ������±����еIJ�ͬʵ�飨������ͬ��ͬѹ�²ⶨ����
![]()
ʵ����� | ����Ͳ������ | ����Ͳ������ | ����Ͳ������ |
1 | 10 mLFeO4��Һ | 10 mLNH3 | ���ɰ�ɫ���������ɫ |
2 | 20 mLH2S | 12mLSO2 | |
3 | 30 mLNO2 | 10 mLH2O(l) | ʣ����ɫ���壬�����Զ�����ѹ�� |
4 | 15 mLCl2 | 40 mLNH3 |
�Իش��������⣺
(1)ʵ��1�У��������ձ�Ϊ_____ɫ��д��������ɫ�Ļ�ѧ����ʽ_________________________��
(2)ʵ��2����Ͳ�ڵ������ǣ���_____________���ɣ�����______�ƶ��������⡢���ڡ�������
��Ӧ�����Ͳ���������IJ������壬��ȷ�Ĵ��������ǽ���ͨ��___________��Һ�С�
(3)ʵ��3�У��������ʣ�����ɫ������_______��д��NO2��H2O��Ӧ�Ļ�ѧ����ʽ_______��
(4)ʵ��4�У���֪��Cl2 + NH3 �� N2+ HCl������Ͳ���������ƶ�����Ͳ���а��̲����⣬�������ɫ�仯Ϊ____________�������Ͳ��ʣ����������ԼΪ_________mL��
����Ŀ������ʵ�������Ԥ��ʵ��Ŀ�Ļ�����ʵ�����һ�µ���
ѡ�� | ʵ����������� | Ԥ��ʵ��Ŀ�Ļ���� |
A | ����֧ʢ��KI3����Һ���Թ��У��ֱ�μӵ�����Һ��AgNO3��Һ��ǰ����Һ�����������л�ɫ���� | KI3��Һ�д���ƽ��:I3 - |
B | �ýྻ�IJ�˿պȡij��Һ�ڻ���������,�۲쵽�����Ի�ɫ | ����Һ��һ������Na+,һ ��û��K+ |
C | ������,�� pH ��ֽ�ֱ�ⶨŨ��Ϊ 0.1mol/L NaClO��Һ�� 0.1mol/L CH3COONa ��Һ��pH | �Ƚ�HC1O ��CH3COOH������ǿ�� |
D | Ũ�������Ҵ�170�����ȣ��Ƶõ�����ͨ������KMnO4 ��Һ����Һ��ɫ��ȥ | �Ƶõ�����Ϊ��ϩ |
A. A B. B C. C D. D