题目内容
5.按题给要求填空:(1)写出以乙炔为原料制备聚氯乙烯反应方程式(无机物不限)
①CH≡CH+HCl→CH2=CHCl.②
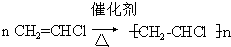 .
.(2)分子式为C6H12 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为(CH3)2C=C(CH3)2,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为CH3C≡CCH3.
分析 (1)乙炔与HCl发生加成反应生成CH2=CHCl,然后CH2=CHCl发生加聚反应生成聚氯乙烯;
(2)由乙烯为平面结构可知,乙烯中4个H被甲基取代后所有C原子共面;由乙炔为直线结构可知,乙炔中H被甲基取代后所有C原子共直线.
解答 解:(1)乙炔与HCl发生加成反应生成CH2=CHCl,然后CH2=CHCl发生加聚反应生成聚氯乙烯,发生的反应分别为CH≡CH+HCl→CH2=CHCl,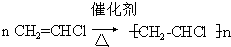 ,
,
故答案为:CH≡CH+HCl→CH2=CHCl;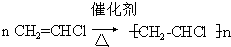 ;
;
(2)由乙烯为平面结构可知,乙烯中4个H被甲基取代后所有C原子共面,则C6H12 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为(CH3)2C=C(CH3)2;由乙炔为直线结构可知,乙炔中H被甲基取代后所有C原子共直线,则C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为CH3C≡CCH3,
故答案为:(CH3)2C=C(CH3)2;CH3C≡CCH3.
点评 本题考查有机物的合成及推断,为高频考点,把握烯烃的性质及常见有机物的结构特点为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.将一定体积质量分数为14%的KOH溶液100g加热蒸发至体积为50mL,冷却至室温无晶体析出,此时溶液的物质的量浓度为( )
| A. | 5mol•L-1 | B. | 6.25mol•L-1 | C. | 7mol•L-1 | D. | 6.75mol•L-1 |
16.下列各组中,分子数目相同的是( )
| A. | 22.4 L氩气和1 mol氢气 | |
| B. | 2 g氢气和16 g氧气 | |
| C. | 同温同压下,2 L氢气和2 L水 | |
| D. | 常温常压下1 mol氧气和标准状况下2 g氢气 |
13.25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A. | 向水中加入稀氨水,平衡逆向移动,[OH-]降低 | |
| B. | 向水中加入少量固体硫酸氢钠,[H+]增大,KW不变 | |
| C. | 将水加热至95℃,pH<7,说明加热可导致水呈酸性 | |
| D. | 将水加热至95℃,仍然呈中性,KW不变 |
20.下列离子方程式,正确的是( )
| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | 过量NaHSO4溶液与少量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 铁与H2SO4反应:Fe+2H+═Fe3++H2↑ | |
| D. | CaCO3溶于稀盐酸中:CO32-+2H+═CO2↑+H2O |
10.实验室可用如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是( )

| A. | NO2 | B. | NO | C. | SO2 | D. | NH3 |
17.下列反应属于吸热反应的是( )
| A. | 铁与盐酸 | B. | 碳与二氧化碳 | C. | 硫酸与氢氧化钠 | D. | 钠与水 |
14.某无色溶液中存在大量的NH4+、H+、NO3ˉ,该溶液中还可能大量存在的离子是( )
| A. | CO32ˉ | B. | OHˉ | C. | Fe2+ | D. | Al3+ |
15.铅酸蓄电池工作时的化学反应方程式为:PbO2+Pb+2H2SO4═2PbSO4+2H2O,则放电过程中被氧化的物质是( )
| A. | PbO2 | B. | Pb | C. | H2SO4 | D. | PbSO4 |