题目内容
17.下列化学物质在实际生产生活和科技等方面的应用不正确的是( )| A. | 次氯酸钠水溶液具有强氧化性,故可用作消毒剂 | |
| B. | 氢氟酸能蚀刻玻璃,是利用氢氟酸的弱酸性 | |
| C. | 常温下,铝能被浓硫酸钝化,可用铝罐贮运浓硫酸 | |
| D. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
分析 A.次氯酸钠水溶液具有强氧化性,能够使蛋白质变性;
B.氢氟酸能够与玻璃中二氧化硅反应生成四氟化硅和水;
C.依据浓硫酸具有强氧化性解答;
D.硫酸钙溶解度小于碳酸钙,依据沉淀转化规律解答.
解答 解:A.次氯酸钠水溶液具有强氧化性,能够使蛋白质变性,可以杀菌消毒,故A正确;
B.氢氟酸能够与玻璃中二氧化硅反应生成四氟化硅和水,能够腐蚀玻璃,所以可以用来雕刻玻璃,与弱酸性无关,故B错误;
C.据浓硫酸具有强氧化性,常温下能够使铝钝化形成致密氧化膜,阻止浓硫酸与铝进一步反应,所以可以铝罐贮运浓硫酸,故C正确;
D.硫酸钙溶解度小于碳酸钙,锅炉水垢中含有的CaSO4,可先加入碳酸钙,使硫酸钙沉淀转化为碳酸钙沉淀,碳酸钙能够溶于酸,可用酸除去,故D正确;
故选:B.
点评 本题考查了物质的用途,性质决定用途,明确物质的用途是解题关键,题目难度不大,注意沉淀转化规则:难溶于水的沉淀可以转化为更难溶于水的物质.

练习册系列答案
相关题目
16.下列实验操作正确的是( )
| A. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| B. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| C. | 先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称 | |
| D. | 萃取,分液前不需对分液漏斗检漏 |
12.硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元.硅氧四面体可以用投影图表示成:其中○表示氧原子,中心黑点表示硅原子.硅氧四面体通过不同方式的连接可以组成各种不同的硅酸根离子.试确定在无限长的单链阴离子中(见下图),硅原子与氧原子的个数之比为( )


| A. | 1:3 | B. | 1:4 | C. | 2:5 | D. | 2:7 |
2.某化学实验小组同学向用大理石和稀盐酸制备CO2后的残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示.下列有关说法不正确的是( )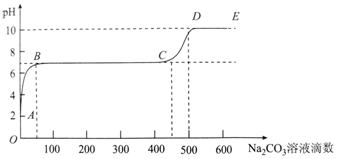

| A. | 开始时溶液pH=2是因为残留液中还有盐酸剩余 | |
| B. | BC段表示随着碳酸钠溶液的滴入,CaCO3沉淀的质量逐渐增加 | |
| C. | AB发生的反应为:Ca2++CO32-═CaCO3↓ | |
| D. | 滴入500滴碳酸钠溶液后溶液中c(OH-)>c(H+) |
9.下图是常用的化学仪器,其中常用于物质的分离与提纯的是( )
| A. |  | B. |  | C. |  | D. |  |
6.32.5gZn投入到VmL浓硫酸中,共热,恰好完全反应,则可以确定的数据是( )
| A. | 所得气体在标准状况下的体积 | B. | 所得气体的质量 | ||
| C. | 所得溶液的浓度 | D. | 原硫酸的浓度 |
 .
.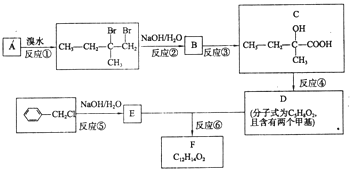 分子式为C12H14O2的有机物F广泛用于制备香精的调香剂.为了合成该有机物,某实验室的科技人员设计了下列合成路线.
分子式为C12H14O2的有机物F广泛用于制备香精的调香剂.为了合成该有机物,某实验室的科技人员设计了下列合成路线. .
.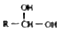 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$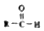 请根据如图回答:
请根据如图回答:
 .
. ;②CH3CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH3COONa+Cu2O+3H2O.
;②CH3CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH3COONa+Cu2O+3H2O.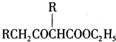 +C2H3OH,请以G为唯一有机试剂合成乙酰乙酸乙酯(CH3COCH2COOC2H5),设计合成路线(其他试剂任选).
+C2H3OH,请以G为唯一有机试剂合成乙酰乙酸乙酯(CH3COCH2COOC2H5),设计合成路线(其他试剂任选).