题目内容
工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为-890.3kJ?mol-1、-285.8kJ?mol-1和-283.0kJ?mol-1,则生成1m3(标准状况)CO所需热量为 .
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:根据CH4、H2、和CO的燃烧热分别写出燃烧的热化学方程式,利用盖斯定律书写高温重整制备CO的热化学方程式,据此计算.
解答:
解:根据CH4、H2、和CO的燃烧热可知,各物质燃烧的热化学方程式:
①O2(g)+2H2(g)=2H2O(L)△H=-571.6kJ?mol -1;
②CH4(g)+2O2(g)=CO2(g)+2H2O(L)△H=-890.3kJ?mol-1;
③2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ?mol-1,
利用盖斯定律将②-①-③可得:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.3 kJ?mol -1,
即生成2molCO,需要吸热247.3 KJ,故得到1立方米的CO吸热为
×
×247.3 KJ=5.52×103KJ,
故答案为:5.52×103KJ.
①O2(g)+2H2(g)=2H2O(L)△H=-571.6kJ?mol -1;
②CH4(g)+2O2(g)=CO2(g)+2H2O(L)△H=-890.3kJ?mol-1;
③2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ?mol-1,
利用盖斯定律将②-①-③可得:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.3 kJ?mol -1,
即生成2molCO,需要吸热247.3 KJ,故得到1立方米的CO吸热为
| 1000L |
| 22.4L/mol |
| 1 |
| 2 |
故答案为:5.52×103KJ.
点评:本题考查反应热的有关计算,难度中等,关键是根据燃烧热与盖斯定律书写高温重整制备CO的热化学方程式.

练习册系列答案
相关题目
A、B、C、D、E 五种芳香化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料.它们的结构简式如下所示:

这五种化合物中,互为同分异构体的是( )

这五种化合物中,互为同分异构体的是( )
| A、B和D | B、A和C |
| C、B和C | D、D和E |
某元素的最高价含氧酸的阴离子符号是RO3-,则该元素的气态氢化物的化学式是( )
| A、HR |
| B、H2R |
| C、RH3 |
| D、不能确定 |

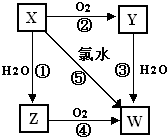 已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化
已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化