题目内容
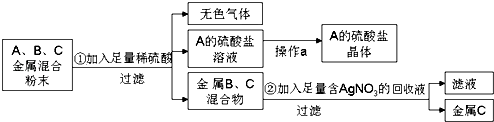
【题目】废旧锂电池正极材料主要含LiCoO2、Al等,以其为原料获得CoC2O4和LiCO3的一种工艺路线如图所示。已知:LiCoO2是不溶于水的固体。

回答下列问题:
(1)滤液①的主要溶质的化学式是_____________。
(2)反应①中过滤时所需的玻璃仪器有___________________。
(3)反应②中LiCoO2与H2O2反应的离子方程式为__________________。
(4)滤液③中含有Na2C2O4,0.1 mol·L-1的Na2C2O4溶液中离子浓度由大到小的顺序是____________。
【答案】 NaAlO2(或NaOH 和 NaA1O2) 烧杯、漏斗、玻璃棒 2LiCoO2+6H++H2O2=2Co2++O2↑+2Li++4H2O c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)
【解析】(1)Al与过量的氢氧化钠反应生成偏铝酸钠,而LiCoO2不与氢氧化钠反应存在于滤渣中,反应滤液①的主要溶质的化学式是NaAlO2或NaOH 和 NaA1O2;(2)过滤操作一般需要烧杯、漏斗、玻璃棒等玻璃仪器;(3)反应②中LiCoO2与H2O2在酸性条件下反应生成钴盐、锂盐、氧气和水,反应的离子方程式为:2LiCoO2+6H++H2O2=2Co2++O2↑+2Li++4H2O;4)滤液③中含有Na2C2O4,Na2C2O4是强碱弱酸盐,C2O42-在水溶液中会水解,且第一步水解比第二步水解程度大,0.1 mol·L-1的Na2C2O4溶液中离子浓度由大到小的顺序是c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表为元素周期表的一部分:
C | N | |||
X | Y | Z | Cl |
回答下列问题:
(1)Y在元素周期表中的位置为__________,X的简单离子结构示意图为_______________。
(2)表中元素中:原子半径最大的是_________(填元素符号),最高价氧化物对应水化物的酸性最强的是______________(填化学式)。
(3)下列事实能说明氯的非金属性比氮强的事实是________(填字母)。
a.Cl2的沸点比N2的高 b.3Cl2+2NH3=6HCl+N2
c.Cl2中原子间为含单键,N2中原子间为三键 d.HCl和NH3受热分解,HCl分解温度高
(4)碳与X可形成化合物M,M的相对分子质量为144。M与盐酸反应的化学方程式为___________。