题目内容
【题目】碘及其化合物主要用于医药、照相及染料等。碘是合成碘化物的基本原料。空气吹出法从卤水中提碘的流程如下:
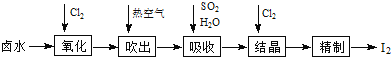
回答下列问题:
(1)“氧化”时,Cl2过量会将I2氧化为HIO3,写出生成HIO3的化学方程式_________;
(2)“吹出”在吹出塔中进行,含碘卤水从_________(填“塔顶”或“塔底”,下同)进入,热空气从_________进入,理由为_________;
(3)吸收塔应选择耐酸材料,原因是_________;
(4)结晶时,发生反应的离子方程式为_________;
(5)从“氧化”所得含碘卤水中提取碘还可以采用加CCl4的方法,该分离方法为_________;为进一步分离I2和CCl4,向其中加入NaOH溶液与I2反应,生成的I-、IO3-进入水溶液;分液后再酸化,即得粗碘.加入NaOH后溶液中I-、IO3-的物质的量之比为_________;
(6)H2O2也能发生与Cl2类似的反应,若先用H2O2将卤水中的I-氧化为IO3-,再将其与卤水按一定比例混合、酸化制取粗碘,处理含I-为254mg/L的卤水1m3,理论上需20%的H2O2_________g。
【答案】 5Cl2+I2+6H2O=2HIO3+10HCl 塔顶 塔底 (热空气密度小)气体与溶液逆向接触时有利于充分接触、提高吹出率 反应生成HI和H2SO4两种强酸 C12+ 2I-=2Cl-+I2 萃取(或萃取、分液) 5:1 170 g
【解析】试题分析:卤水中碘和氯气发生氧化还原反应生成HCl和HIO3,反应物的接触时间越长,反应越充分,所以含碘卤水应该从塔顶加入,热空气从塔底加入,向剩余液体中加入二氧化硫和水,发生氧化还原反应生成HI和硫酸,再向溶液中通入足量氯气,氯气将HI氧化生成碘单质,最后通过精制得到碘单质。
(1)氯气、碘在水溶液中发生氧化还原反应生成碘酸和HCl,反应方程式为5Cl2+I2+6H2O=2HIO3+10HCl,故答案为:5Cl2+I2+6H2O=2HIO3+10HCl;
(2)反应物接触时间越长,反应越充分,热空气密度小,且气体与溶液逆向接触,有利于提高吹出率,所以含碘卤水从塔顶进入,热空气从塔底进入,故答案为:塔顶;塔底;因热空气密度小,且气体与溶液逆向接触,有利于提高吹出率;
(3)碘和二氧化硫在水溶液中能发生氧化还原反应生成HI和H2SO4两种强酸,酸能腐蚀某些物质,所以吸收塔应选择耐酸材料,故答案为:反应生成HI和H2SO4两种强酸;
(4)结晶时,通入氯气,将溶液中的碘离子置换出来,反应的离子方程式为,C12+ 2I-=2Cl-+I2,故答案为:C12+ 2I-=2Cl-+I2;
(5)碘在四氯化碳中的溶解度远远大于在水中的溶解度且碘和四氯化碳不反应,四氯化碳和水不互溶,所以可以采用萃取方法分离;NaOH溶液与I2反应,生成的I-、IO3-进入水溶液,离子反应方程式为6OH-+3I2=5I-+IO3-+3H2O,根据方程式知,加入NaOH后溶液中I-、IO3-的物质的量之比为5:1,故答案为:萃取;5:1;
(6)1m3的254mg/L的卤水中n(I-)=![]() =2mol,H2O2将卤水中的I-氧化为IO3-,发生的反应为3H2O2+I-=3H2O+IO3-①,酸性条件下,I-和碘酸根离子反应方程式为5I-+IO3-+6H+=3I2+3H2O②,
=2mol,H2O2将卤水中的I-氧化为IO3-,发生的反应为3H2O2+I-=3H2O+IO3-①,酸性条件下,I-和碘酸根离子反应方程式为5I-+IO3-+6H+=3I2+3H2O②,
根据方程式②知参加反应的I-和IO3-的关系是5:1,根据I原子守恒得发生反应①消耗I-与生成IO3-关系为1:1,所以反应①中消耗I-的物质的量占总的![]() 为2mol×
为2mol×![]() =
=![]() mol,则消耗n(H2O2)=3×
mol,则消耗n(H2O2)=3×![]() mol=1mol,理论上需20%的H2O2=
mol=1mol,理论上需20%的H2O2=![]() =170g,故答案为:170。
=170g,故答案为:170。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案