题目内容
往下列溶液中,通入足量CO2气体,最终能析出固体的是
| A.澄清石灰水 | B.饱和Na2CO3溶液 | C.CaCl2溶液 | D.盐酸 |
B
解析试题分析:A、足量二氧化碳与澄清石灰水反应先有沉淀后消失,错误;B、二氧化碳与碳酸钠反应生成碳酸氢钠,而碳酸氢钠的溶解度小于碳酸钠,所以在饱和碳酸钠溶液中通二氧化碳会有碳酸氢钠固体析出,正确;C、二氧化碳不与氯化钙溶液反应,错误;D、二氧化碳不与盐酸反应,错误,答案选B。
考点:考查二氧化碳的化学性质

 考前必练系列答案
考前必练系列答案设空气中O2的体积分数为0.2,N2的体积分数为0.8。在有水存在的条件下,某氮的氧化物(NO与NO2形成的混合物)和一定量空气混合恰好完全反应生成硝酸,反应后气体体积减少了一半(相同条件下)。则该氮的氧化物中NO与NO2的体积比可能是
| A.1∶5 | B.1∶4 |
| C.1∶3 | D.任意比 |
一定温度下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1 mol·L-1的NaOH溶液,溶液pH变化的曲线如图所示。下列叙述中正确的是( )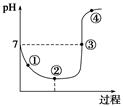
| A.①点的溶液中:c(H+)=c(Cl-)+c(HClO)+c(OH-) |
| B.②点的溶液中:c(H+)>c(Cl-)>c(ClO-)>c(HClO) |
| C.③点的溶液中:c(Na+)=2c(ClO-)+c(HClO) |
| D.④点的溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(HClO) |
实验室既可用浓盐酸与MnO2在加热时反应制备Cl2,也可用KMnO4与浓盐酸在常温下反应制备Cl2,下列有关说法中不正确的是( )
| A.由题目信息知:KMnO4的氧化性比MnO2的强 |
| B.制备氯气的整个实验过程中,只需要使用氧化剂与还原剂 |
| C.用排气法收集不需要利用其他试剂就能确定集气瓶中已收集满气体 |
| D.用足量MnO2与含有4 mol HCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1 mol |
下列说法正确的是( )
| A.硅材料广泛应用光纤通讯 |
| B.工艺师利用盐酸刻蚀石英制作艺术品 |
| C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D.粗硅制备单晶硅不涉及氧化还原反应 |
青石棉(cricidolite)是世界卫生组织确认的一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,青石棉的化学式为Na2Fe5Si8O22(OH)2,青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法不正确的是 ( )。
| A.青石棉是一种易燃品且易溶于水 |
| B.青石棉的化学组成用氧化物的形式可表示为Na2O·3FeO·Fe2O3·8SiO2·H2O |
| C.1 mol Na2Fe5Si8O22(OH)2与足量的硝酸作用,至少需消耗6 L 3 mol·L-1的硝酸 |
| D.Na2Fe5Si8O22(OH)2能与氢氟酸作用 |
世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“中国至少在距今3 000年以前,就已经使用玻璃了。”下列有关玻璃的说法不正确的是( )
| A.制普通玻璃的原料主要是纯碱、石灰石和石英 |
| B.玻璃在加热熔化时有固定的熔点 |
| C.普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅 |
| D.盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅生成硅酸钠而使瓶塞与瓶口粘在一起 |
卤素是最活泼的一族非金属,下列关于卤族元素的说法正确的是( )
| A.卤素单质的最外层电子数都是7 |
| B.从上到下,卤素原子的电子层数依次增多,半径依次减小 |
| C.从F到I,原子核对最外层电子的吸引能力依次减弱,原子得电子能力依次减弱 |
| D.卤素单质与H2化合的容易程度为F2<Cl2<Br2<I2 |
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如下图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )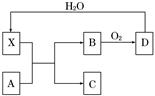
| A.X使蔗糖变黑的现象主要体现了X的强氧化性 |
| B.若A为铁,则足量A与X在室温下即可完全反应 |
| C.若A为碳单质,则将C通入少量的澄清石灰水,一定可以观察到白色沉淀产生 |
| D.工业上,B转化为D的反应条件为高温、常压、使用催化剂 |