题目内容
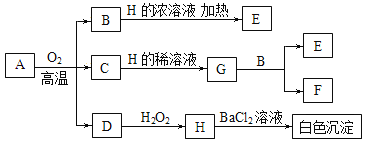
【题目】化合物A中含有三种元素,3.68gA在氧气中充分锻烧后生成1.28g B、1.60g C和气体D。物质A~H存在如下转化关系。已知B是一种红色固体单质,C是金属氧化物,D是非金属氧化物,E、F、G是盐。
请回答:
(1)检验气体D的实验方法:____________________。
(2)写出B与H浓溶液反应的化学方程式:____________________。
(3)化合物A的化学式:____________________。
【答案】 将气体通入品红溶液,红色褪色,加热溶液,溶液红色恢复,即是SO2气体 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O FeCuS2
CuSO4+SO2↑+2H2O FeCuS2
【解析】B是一种红色固体单质,则B为Cu,Cu通常只能溶解于热的浓硫酸、浓硝酸或稀硝酸,其中H中含有SO42-,则H为硫酸;Cu溶解于浓硫酸生成CuSO4,C是金属氧化物,溶解于稀硫酸,生成的盐能溶解Cu生成硫酸铜和另一种盐F,则C为氧化铁,G为硫酸铁,F为硫酸亚铁;D是非金属氧化物,于过氧化氢反应生成硫酸,则D为SO2;
(1)SO2有漂白性和还原性,可将气体通入品红溶液,红色褪色,加热溶液,溶液红色恢复,即是SO2气体;
(2)Cu溶解于浓硫酸发生反应的化学方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(3)3.68gA在氧气中充分锻烧后生成1.28gCu、1.60g Fe2O3和气体SO2,则A中含有的Cu为![]() =0.02mol,Fe为
=0.02mol,Fe为![]() =0.02mol,S元素为
=0.02mol,S元素为![]() =0.04mol,Cu、Fe、S的原子数目比为0.02mol:0.02mol:0.04mol=1:1:2,则化合物A的化学式为FeCuS2。
=0.04mol,Cu、Fe、S的原子数目比为0.02mol:0.02mol:0.04mol=1:1:2,则化合物A的化学式为FeCuS2。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目