题目内容
某溶液中含有的离子可能是K+、Ba2+、A13+、Mg2+、AlO2-、CO32-、SiO32-、Cl-中的几种,现进行如下实验:
①取少量溶液加氢氧化钠溶液过程中无沉淀生成
②另取少量原溶液,逐滴加入5 mL0.2 mol·L-1盐酸,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失。
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.43 g。
下列说法中正确的是:
| A.该溶液中一定不含Ba2+ 、Mg2+、A13+、SiO32-、Cl- |
| B.该溶液中一定含有K+、AlO2-、CO32-、Cl- |
| C.该溶液是否有K+ 需做焰色反应(透过蓝色钴玻璃片) |
| D.可能含有Cl- |
B
解析试题分析:根据①判断溶液溶液中无A13+、Mg2+;根据②判断溶液中含有AlO2-、CO32-,不含SiO32-,因碳酸钡沉淀,得出不含有Ba2+;阳离子只有K+,一定含有;根据③计算n(Cl-)=0.43÷143.5=0.003mol,盐酸提供的n(Cl-)=0.2×0.005=0.001mol,故原溶液中含有氯离子。
考点:考查离子共存与检验有关问题。

下列反应的离子方程式,正确的是( )
A.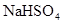 溶液与 溶液与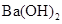 溶液混合: 溶液混合: ↓ ↓ |
B.醋酸除水垢: ↑+ ↑+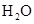 |
C.漂白粉溶液中通入过量的 ↓+ ↓+ |
D.少量金属钠放入冷水中: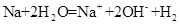 ↑ ↑ |
某溶液中可能存在Fe3+、Fe2+、I-、HCO3-、Cl-、NO3-六种离子中的几种。进行下列实验:
①取少量溶液滴加KSCN溶液,溶液呈血红色;
②另取少量原溶液滴加盐酸,溶液的棕黄色加深。
据此可以推断,该溶液中肯定不能大量存在的离子是
| A.I- | B.HCO3- | C.Fe2+ | D.NO3- |
在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,反应完全后,离子数目几乎没有变化的是
| A.Fe3+ | B.Fe2+ | C.Al3+ | D.NH4+ |
下列各组中两种物质在溶液的反应,能用同一离子方程式表示的是
| A.铁和稀盐酸、铁和稀硝酸 |
| B.铜和浓硝酸、铜和稀硝酸 |
| C.NaHCO3+ NaOH;NaHSO4+ NaOH |
| D.BaCl2+ H2SO4; Ba(OH)2+ Na2SO4 |
常温下,在c(H+)/c(OH?)=1×1012的溶液中,下列各组离子能大量共存的是
| A.Fe2+、Mg2+、NO3?、SO42? | B.Fe3+、Na+、Cl?、SCN? |
| C.NH4+、Al3+、NO3?、Cl? | D.Ca2+、K+、Cl?、HCO3? |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使甲基橙变红的溶液:Fe2+、K+、SO42-、NO3- |
| B.加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- |
| C.0.1 mol·L-1NaAlO2溶液:Al3+、Na+、Cl-、NO3- |
| D.水电离出的c(H+)=10-12 mol·L-1的溶液:Na+、K+、NH4+、CO32- |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.无色溶液中:K+、Fe3+、SO42-、SCN- |
| C.c (H+)/c (OH-) = 1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.由水电离的c (H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
下列各组离子在溶液中能大量共存的是
| A.Na+、Ba2+、OH—、Cl— | B.Na+、NH4+、OH—、HCO3— |
| C.NH4+、A13+、SiO32—、CO32ˉ | D.H+、Ag+、Cl—、ClO— |